题目内容
(8分)有一瓶澄清溶液,其中只可能含有Na+ 、NH4+ 、Mg2+ 、Ba2+ 、Fe3+ 、Cl— 、SO42—、CO32— 离子(不考虑H+、OH—)。取该溶液进行以下实验:
(1)用pH试纸检验溶液,溶液呈酸性,
(2)另取部分溶液滴入NaOH溶液,使溶液从酸性逐渐变成碱性,无沉淀产生,
(3)取(2)中部分碱性溶液,滴加Na2CO3溶液,有白色沉淀析出,
(4)将(2)中剩余碱性溶液加热,有气体放出,该气体能使润湿的红色石蕊试纸变蓝色。
根据上述实验事实确定:
①该溶液中肯定存在的离子是 ;
②肯定不存在的离子是 ;
③可能存在的离子是 。
(8分)① Ba2+、NH4+、Cl— (3分); ②Mg2+、Fe3+、CO32—、SO42—(4分);
③Na+(1分))
【解析】
试题分析:(1)用pH试纸检验溶液,溶液呈酸性,则含有H+,由于H+与CO32—会发生离子反应而不能大量共存,所以不含CO32—;(2)另取部分溶液滴入NaOH溶液,使溶液从酸性逐渐变成碱性,无沉淀产生,说明不含Mg2+ 、Fe3+;(3)取(2)中部分碱性溶液,滴加Na2CO3溶液,有白色沉淀析出,该沉淀是BaCO3,含有Ba2+;由于Ba2+与SO42—会发生离子反应而不能大量共存,因此无SO42—;(4)将(2)中剩余碱性溶液加热,有气体放出,该气体能使润湿的红色石蕊试纸变蓝色,证明含有NH4+。根据溶液呈电中性的原理可知。该溶液中还含有Cl—。所以①该溶液中肯定存在的离子是Ba2+、NH4+、Cl—;②肯定不存在的离子是Mg2+、Fe3+、CO32—、SO42—;③在上述实验中没有涉及的离子是Na+,它可能存在,也可能不存在,故可能存在的离子是Na+。
考点:考查离子的鉴定一离子共存的知识。

 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案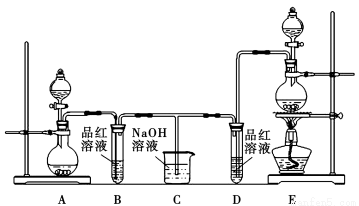
 MnCl2+2H2O+Cl2↑,应选用上图A、E装置中的______________(填序号)制Cl2,反应中浓盐酸所表现出的性质是__________________。
MnCl2+2H2O+Cl2↑,应选用上图A、E装置中的______________(填序号)制Cl2,反应中浓盐酸所表现出的性质是__________________。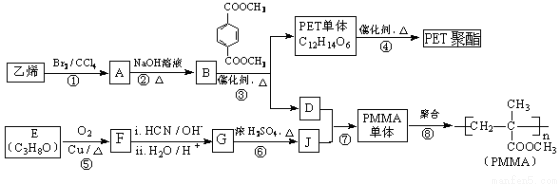
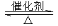 RCO18OR’’+R’OH(R、R’、R’’代表烃基)
RCO18OR’’+R’OH(R、R’、R’’代表烃基) Ⅱ.
Ⅱ.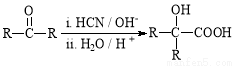 (R、R’代表烃基)
(R、R’代表烃基) 与足量NaOH溶液反应时,最多消耗4 mol NaOH
与足量NaOH溶液反应时,最多消耗4 mol NaOH