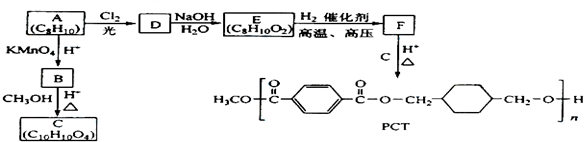
题目内容
硫在地壳中主要以硫化物、硫酸盐等形式存在,其单质和化合物在工农业生产中有着重要的应用.(1)已知:重晶石(BaSO4)高温煅烧可发生一系列反应,其中部分反应如下:
BaSO4(s)+4C(s)=BaS(s)+4CO(g)△H=+571.2kJ?mol-1
BaS(s)=Ba(s)+S(s)△H=+460kJ?mol-1
已知:2C(s)+O2(g)=2CO(g)△H=-221kJ?mol-1则Ba(s)+S(s)+2O2(g)=BaSO4(s)△H= .
(2)雄黄(As4S4)和雌黄(As2S3)是提取砷的主要矿物原料.已知As2S3和HNO3有如下反应:
As2S3+10H++10NO3-=2H3AsO4+3S+10NO2↑+2H2O
当反应中转移电子的数目为2mol时,生成H3AsO4的物质的量为 .
(3)向等物质的量浓度Na2S、NaOH混合溶液中滴加稀盐酸至过量.其中主要含硫各物种(H2S、HS-、S2-)的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与滴加盐酸体积的关系如图1所示(忽略滴加过程H2S气体的逸出).
①含硫物种B表示 .在滴加盐酸过程中,溶液中c(Na+)与含硫各物种浓度的大小关系为 (填字母).
a.c(Na+)=c(H2S)+c(HS-)+2c(S2-)
b.2c(Na+)=c(H2S)+c(HS-)+c(S2-)
c.c(Na+)=3[c(H2S)+c(HS-)+c(S2-)]
②NaHS溶液呈碱性,若向溶液中加入CuSO4溶液,恰好完全反应,所得溶液呈强酸性,其原因是 (用离子方程式表示).
(4)硫的有机物( )与甲醛、氯化氢以物质的量之比1:1:1反应,可获得一种杀虫剂中间体X和H2O.
)与甲醛、氯化氢以物质的量之比1:1:1反应,可获得一种杀虫剂中间体X和H2O. 及X的核磁共振氢谱如图2,其中 (填“Ⅰ”或“Ⅱ”)为
及X的核磁共振氢谱如图2,其中 (填“Ⅰ”或“Ⅱ”)为 的核磁共振氢谱图.写出X的结构简式: .
的核磁共振氢谱图.写出X的结构简式: .

BaSO4(s)+4C(s)=BaS(s)+4CO(g)△H=+571.2kJ?mol-1
BaS(s)=Ba(s)+S(s)△H=+460kJ?mol-1
已知:2C(s)+O2(g)=2CO(g)△H=-221kJ?mol-1则Ba(s)+S(s)+2O2(g)=BaSO4(s)△H=
(2)雄黄(As4S4)和雌黄(As2S3)是提取砷的主要矿物原料.已知As2S3和HNO3有如下反应:
As2S3+10H++10NO3-=2H3AsO4+3S+10NO2↑+2H2O
当反应中转移电子的数目为2mol时,生成H3AsO4的物质的量为
(3)向等物质的量浓度Na2S、NaOH混合溶液中滴加稀盐酸至过量.其中主要含硫各物种(H2S、HS-、S2-)的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与滴加盐酸体积的关系如图1所示(忽略滴加过程H2S气体的逸出).
①含硫物种B表示
a.c(Na+)=c(H2S)+c(HS-)+2c(S2-)
b.2c(Na+)=c(H2S)+c(HS-)+c(S2-)
c.c(Na+)=3[c(H2S)+c(HS-)+c(S2-)]
②NaHS溶液呈碱性,若向溶液中加入CuSO4溶液,恰好完全反应,所得溶液呈强酸性,其原因是
(4)硫的有机物(
 )与甲醛、氯化氢以物质的量之比1:1:1反应,可获得一种杀虫剂中间体X和H2O.
)与甲醛、氯化氢以物质的量之比1:1:1反应,可获得一种杀虫剂中间体X和H2O. 及X的核磁共振氢谱如图2,其中
及X的核磁共振氢谱如图2,其中 的核磁共振氢谱图.写出X的结构简式:
的核磁共振氢谱图.写出X的结构简式:
考点:热化学方程式,氧化还原反应的计算,离子共存问题,有机物实验式和分子式的确定
专题:
分析:(1)已知①BaSO4(s)+4C(s)=BaS(s)+4CO(g)△H=+571.2kJ?mol-1
②BaS(s)=Ba(s)+S(s)△H=+460kJ?mol-1
③2C(s)+O2(g)=2CO(g)△H=-221kJ?mol-1,
根据盖斯定律:③×2-①-②得方程式Ba(s)+S(s)+2O2(g)=BaSO4(s)据此计算.
(2)根据化合价的升降以及物质的量的情况来计算转移电子的量;
(3)①向等物质的量浓度Na2S、NaOH混合溶液中滴加稀盐酸,盐酸和氢氧化钠先反应,然后和硫化钠反应,结合图1所示H2S、HS-、S2-的分布分数进行解答;NaHS的含量先增加后减少;根据物料守恒可求得滴加过程中,溶液中微粒浓度大小关系;
②NaHS溶液中加入CuSO4溶液,会发生反应生成硫化铜和酸;
(4)核磁共振氢谱图可以确定氢原子的种类和数目,据此确定分子式.
②BaS(s)=Ba(s)+S(s)△H=+460kJ?mol-1
③2C(s)+O2(g)=2CO(g)△H=-221kJ?mol-1,
根据盖斯定律:③×2-①-②得方程式Ba(s)+S(s)+2O2(g)=BaSO4(s)据此计算.
(2)根据化合价的升降以及物质的量的情况来计算转移电子的量;
(3)①向等物质的量浓度Na2S、NaOH混合溶液中滴加稀盐酸,盐酸和氢氧化钠先反应,然后和硫化钠反应,结合图1所示H2S、HS-、S2-的分布分数进行解答;NaHS的含量先增加后减少;根据物料守恒可求得滴加过程中,溶液中微粒浓度大小关系;
②NaHS溶液中加入CuSO4溶液,会发生反应生成硫化铜和酸;
(4)核磁共振氢谱图可以确定氢原子的种类和数目,据此确定分子式.
解答:
解:(1)已知①BaSO4(s)+4C(s)=BaS(s)+4CO(g)△H=+571.2kJ?mol-1
②BaS(s)=Ba(s)+S(s)△H=+460kJ?mol-1
③2C(s)+O2(g)=2CO(g)△H=-221kJ?mol-1,
根据盖斯定律:③×2-①-②得方程式Ba(s)+S(s)+2O2(g)=BaSO4(s)△H=(-221)×2-(+460)-(+571.2)=-1473.2KJ?mol-1,
故答案为:-1473.2KJ?mol-1.-1473.2 kJ?mol-1;
(2)反应As2S3+10HNO3=2H3AsO4+3S+10NO2↑+2H2O中,As元素化合价由As2S3+3价升高到H3AsO4+5价,S元素化合价由As2S3-2价升高到S,0价,若生成2molH3AsO4,则反应中转移电子的物质的量为10mol,当反应中转移电子的数目为2mol时,生成H3AsO4的物质的量为0.4mol,
故答案为:0.4mol;
(3)①向等物质的量浓度Na2S、NaOH混合溶液中滴加稀盐酸,盐酸和氢氧化钠先反应,然后和硫化钠反应,A表示含硫微粒浓度减小为S2-,B先增加后减少为HS-,C浓度一直在增加为H2S,向等物质的量浓度Na2S、NaOH混合溶液中滴加稀盐酸,因体积相同,设Na2S、NaOH各为1mol,则n(Na)=3n(S),溶液中含硫的微粒为HS-、S2-、H2S,则c(Na+)=3[c(H2S)+c(HS-)+c(S2-)],或溶液中存在电荷守恒得到c(Na+)=c(Cl-)+c(OH-)+c(HS-)+2c(S2-)-c(H+);
故答案为:HS-;c;
②NaHS溶液中加入CuSO4溶液,会发生反应Cu2++HS-=CuS↓+H+,溶液显示强酸性,故答案为:Cu2++HS-=CuS↓+H+,;
(4) 中含有三种类型的氢原子,氢原子的数目之比是1:2:2,所以核磁共振氢谱图Ⅰ符合,硫的有机物(
中含有三种类型的氢原子,氢原子的数目之比是1:2:2,所以核磁共振氢谱图Ⅰ符合,硫的有机物( )与甲醛、氯化氢以物质的量之比1:1:1反应,可获得一种杀虫剂中间体X和H2O.可以确定X的化学式为:C7H6SCl2,核磁共振氢谱图显示存在三种类型的氢原子,各种氢原子个数之比是1:1:1,所以结构简式为:
)与甲醛、氯化氢以物质的量之比1:1:1反应,可获得一种杀虫剂中间体X和H2O.可以确定X的化学式为:C7H6SCl2,核磁共振氢谱图显示存在三种类型的氢原子,各种氢原子个数之比是1:1:1,所以结构简式为: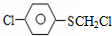 .
.
故答案为:Ⅰ; .
.
②BaS(s)=Ba(s)+S(s)△H=+460kJ?mol-1
③2C(s)+O2(g)=2CO(g)△H=-221kJ?mol-1,
根据盖斯定律:③×2-①-②得方程式Ba(s)+S(s)+2O2(g)=BaSO4(s)△H=(-221)×2-(+460)-(+571.2)=-1473.2KJ?mol-1,
故答案为:-1473.2KJ?mol-1.-1473.2 kJ?mol-1;
(2)反应As2S3+10HNO3=2H3AsO4+3S+10NO2↑+2H2O中,As元素化合价由As2S3+3价升高到H3AsO4+5价,S元素化合价由As2S3-2价升高到S,0价,若生成2molH3AsO4,则反应中转移电子的物质的量为10mol,当反应中转移电子的数目为2mol时,生成H3AsO4的物质的量为0.4mol,
故答案为:0.4mol;
(3)①向等物质的量浓度Na2S、NaOH混合溶液中滴加稀盐酸,盐酸和氢氧化钠先反应,然后和硫化钠反应,A表示含硫微粒浓度减小为S2-,B先增加后减少为HS-,C浓度一直在增加为H2S,向等物质的量浓度Na2S、NaOH混合溶液中滴加稀盐酸,因体积相同,设Na2S、NaOH各为1mol,则n(Na)=3n(S),溶液中含硫的微粒为HS-、S2-、H2S,则c(Na+)=3[c(H2S)+c(HS-)+c(S2-)],或溶液中存在电荷守恒得到c(Na+)=c(Cl-)+c(OH-)+c(HS-)+2c(S2-)-c(H+);
故答案为:HS-;c;
②NaHS溶液中加入CuSO4溶液,会发生反应Cu2++HS-=CuS↓+H+,溶液显示强酸性,故答案为:Cu2++HS-=CuS↓+H+,;
(4)
 中含有三种类型的氢原子,氢原子的数目之比是1:2:2,所以核磁共振氢谱图Ⅰ符合,硫的有机物(
中含有三种类型的氢原子,氢原子的数目之比是1:2:2,所以核磁共振氢谱图Ⅰ符合,硫的有机物( )与甲醛、氯化氢以物质的量之比1:1:1反应,可获得一种杀虫剂中间体X和H2O.可以确定X的化学式为:C7H6SCl2,核磁共振氢谱图显示存在三种类型的氢原子,各种氢原子个数之比是1:1:1,所以结构简式为:
)与甲醛、氯化氢以物质的量之比1:1:1反应,可获得一种杀虫剂中间体X和H2O.可以确定X的化学式为:C7H6SCl2,核磁共振氢谱图显示存在三种类型的氢原子,各种氢原子个数之比是1:1:1,所以结构简式为: .
.故答案为:Ⅰ;
 .
.
点评:本题涉及盖斯定律的应用、氧化还原反应以及溶液中离子浓度之间的关系、有机物的结构等知识的考查,综合性强,难度中等.

练习册系列答案
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案
相关题目
体积相同、pH相同的盐酸和醋酸溶液,再用氢氧化钠溶液中和时,两者消耗氢氧化钠的物质的量是( )
| A、相同 | B、盐酸多 |
| C、醋酸多 | D、无法比较 |
部分氧化的Fe-Cu合金样品(氧化产物为Fe2O3、CuO)共5.92g,经如下处理:下列说法正确的是( )
①滤液A中的阳离子为Fe2+、Fe3+、H+?
②样品中含氧元素的物质的量为0.03mol
③溶解样品的过程中消耗硫酸的总物质的量为0.04mol?
④V=224mL?
⑤V=336mL

①滤液A中的阳离子为Fe2+、Fe3+、H+?
②样品中含氧元素的物质的量为0.03mol
③溶解样品的过程中消耗硫酸的总物质的量为0.04mol?
④V=224mL?
⑤V=336mL

| A、①③④ | B、②③④ |
| C、②③⑤ | D、①③ |
等体积、等pH的盐酸和醋酸,与NaOH中和时,消耗NaOH的量( )
| A、相同 | B、盐酸多 |
| C、醋酸多 | D、无法比较 |
在相同状况下,将下列四种混合气体:①体积比为3:1的NH3和N2,②体积比为1:1的NO和NO2,③体积比为1:1的NO2和O2,④体积比为4:3的NO和O2.分别置于完全相同的试管里,并倒置与谁操着,充分反应后,液面上升的高度分别为h1 h2 h3 h4,下列关系正确的是( )
| A、h1>h2>h3>h4 |
| B、h4>h3>h1>h2 |
| C、h4>h1>h3>h2 |
| D、h2>h3>h1>h4 |