题目内容
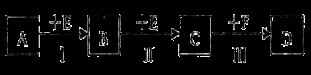
把物质的量均为0.1 mol的AlCl3、CuCl2和H2SO4溶于水制成100 mL的混合溶液,用石墨作电极电解,并收集两电极所产生的气体,一段时间后在两极收集到的气体在相同条件下体积相同。则下列描述正确的是
A.阳极得到的气体中有O2且为0.35 mol
B.铝元素仅以Al(OH)3的形式存在
C.阴极质量增加3.2 g
D.电路中共转移0.9 mol电子
D
【解析】
试题分析:根据离子的放电顺序,则在阴极放电的离子先是Cu2+, Cu2++2e-==Cu,其次是氢离子,发生2H++2e-==H2↑;在阳极放电的首先是氯离子,发生2Cl--2e-=Cl2↑,其次是氢氧根离子,发生2H2O -4e- =O2↑+4H+。根据题意,溶液中Cu2+的物质的量是0.1mol,氢离子的物质的量是0.2mol,氯离子的物质的量是0.5mol,一段时间后在两极收集到的气体在相同条件下体积相同,因为氢离子放电产生的氢气与氯离子放电产生的氯气的体积相等,所以阳极一定有氧气生成,所以阳极的氯离子一定放电完全。设阳极产生氧气的物质的量是x,则阳极:失去电子的物质的量是0.5mol+4x;则阴极产生氢气的物质的量是0.5mol/2+x,所以阴极:得到电子的物质的量是0.1mol×2+(0.5mol/2+x)×2,根据得失电子守恒,有0.5mol+4x=0.1mol×2+(0.5mol/2+x)×2,解得x=0.1mol。A、阳极得到的气体中有0.1mol氧气,错误;B、因为生成氢气的物质的量是0.35mol,则最终溶液呈碱性,硫酸根离子不放电,则铝元素以铝离子和氢氧化铝形式共同存在,错误;C、阴极增加的质量是0.1molCu的质量,为6.4g,错误;D、根据以上计算,电路中转移电子的物质的量是0.5mol+4x=0.9mol,正确,答案选D。
考点:考查电解原理的应用,离子放电顺序的判断,简单计算

 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南大学出版社系列答案
同步练习西南大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
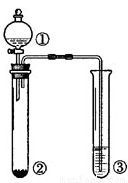
学练快车道口算心算速算天天练系列答案利用图中所示装置进行下列实验,能得出相应实验结论的是
选项 | ① | ② | ③ | 实验结论 |
|
A | 浓盐酸 | MnO2 | NaOH | 制氯气并吸收尾气 | |
B | 浓硫酸 | 蔗糖 | 溴水 | 浓硫酸具有脱水性、氧化性 | |
C | 稀盐酸 | Na2SO3 | Ba(NO3)2溶液 | SO2与可溶性钡盐均可生成白色沉淀 | |
D | 浓硝酸 | Na2CO3 | Na2SiO3溶液 | 酸性:硝酸>碳酸>硅酸 |
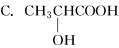
现有一瓶乙二醇和丙三醇的混合物,已知它们的性质如下表,据此,将乙二醇和丙三醇互相分离的最佳方法是
物质 | 分子式 | 熔点(℃) | 沸点(℃) | 密度 | 溶解性 |
乙二醇 | C2H6O2 | -11.5 | 198 | 1.11 | 易溶于水和乙醇 |
丙三醇 | C3H8O3 | 17.9 | 290 | 1.26 | 能跟水和酒精以任意比互溶 |
A.萃取法 B.结晶法 C.分液法 D.蒸馏法