题目内容
实验测得溶液中仅含有SO42-、K+、Cu2+、Cl-,K+、Cu2+、Cl-的个数比为4:5:8,则K+与SO42-的个数比为 .
考点:物质的量的相关计算
专题:计算题
分析:根据溶液中阴阳离子所带正负电荷总数相等判断,已知其中七种离子的个数比,由此计算出K+与SO42-的个数比.
解答:
解:根据溶液中阴阳离子所带正负电荷总数相等,设K+、Cu2+、Cl-个数分别为4、5、8,则所带正电荷总数为14个,所以负电荷总数也必须为14个,其中Cl-带的负电荷为8,所以硫酸根离子所带的负电荷为6,所以SO42-的数值为3,所以K+与SO42-的个数比为4:3,
故答案为:4:3.
故答案为:4:3.
点评:根据溶液中阴阳离子所带正负电荷总数相等判断即可,难度不大,注意基础知识的积累.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
 已知
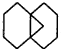
已知  可简写为
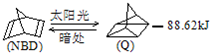
可简写为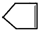 利用某些有机物之间的转化可贮存太阳能,如原降冰片二烯(NBD)经太阳光照转化成四环烷(Q)的反应为如图所示下列有关说法不正确的是( )
利用某些有机物之间的转化可贮存太阳能,如原降冰片二烯(NBD)经太阳光照转化成四环烷(Q)的反应为如图所示下列有关说法不正确的是( )| A、物质Q比NBD更稳定 |
| B、物质Q的一氯取代物只有3种 |
| C、一定条件下,1 mol NBD最多可与2 mol Br2发生加成反应 |
| D、NBD和Q二者互为同分异构体 |
在一定温度下,将等量的气体分别通入起始体积相同的密闭容器I(恒容)和Ⅱ(恒压)中,使其发生反应,t.时容器I中达到化学平衡,x、Y、z的物质的量的变化如图所示,则下列有关推断正确的是( )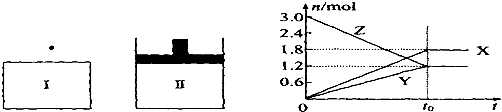

| A、该反应的化学方程式为:3X+2Y?3Z |
| B、若两容器中均达到平衡后,两容器的体积V(I)<V(Ⅱ),则容器Ⅱ达到平衡所用时间小于t |
| C、若两容器中均达到平衡时,两容器中Z的物质的量分数相同,则Y为固态或液态 |
| D、达平衡后,若对容器Ⅱ升高温度时其体积增大,说明Z发生的反应为吸热反应 |
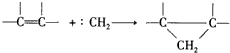
 .
.