题目内容
17.设NA表示阿伏加德罗常数的值,下列说法正确的是( )| A. | 常温常压,22.4 SO3中的硫原子数目大于NA | |
| B. | 50g质量分数为34%的过氧化氢水溶液中含氧原子数目为NA | |
| C. | 5.6g Fe在0.1mol Cl2中充分燃烧,转移的电子数为0.3NA | |
| D. | 0.2mol AlCl3中含离子数为0.8NA |
分析 A.常温常压,三氧化硫为液体;
B.过氧化氢溶液中过氧化氢、水分子都含有氧原子;
C.氯气与铁反应生成氯化铁,氯气少量依据氯气的量计算转移电子数;
D.氯化铝为共价化合物.
解答 解:A.常温常压,三氧化硫为液体,22.4 LSO3物质的量远远大于1mol,硫原子个数大于NA,故A正确;
B.过氧化氢溶液中过氧化氢、水分子都含有氧原子,所以50g质量分数为34%的过氧化氢水溶液中含氧原子数目大于NA,故B错误;
C.5.6g Fe在0.1mol Cl2中充分燃烧生成氯化铁,氯气少量全部分反应生成0.2mol氯离子,转移的电子数为0.2NA,故C错误;
D.氯化铝为共价化合物,不含铝离子,故D错误;
故选:A.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的运用以及物质的状态和结构是解题关键,难度不大,注意气体摩尔体积使用条件和对象.

练习册系列答案
 优等生题库系列答案
优等生题库系列答案
相关题目
8.设NA为阿伏加德罗常数值,下列有关叙述正确的是( )
| A. | 56g铁高温下与足量水蒸气充分反应转移电子数目为3NA | |
| B. | 100 g CaCO3和KHCO3混合固体中CO32-的数目为NA | |
| C. | 实验室用H2O2制备1mol O2转移的电子数为2NA | |
| D. | 标准状况下,2.24L CCl4含有的原子数为0.5NA |
5.下列说法正确的是( )
| A. | IA族元素的金属性比IIA族元素的金属性强 | |
| B. | HF、HCl、HBr、HI的还原性从左到右依次增强 | |
| C. | 同周期非金属氧化物对应的水化物的酸性从左到右依次增强 | |
| D. | 第三周期元素的离子半径从左到右逐渐减小 |
12.下列关于有机物的说法正确的是( )
| A. | CH4和C12按体积比1:3混合可制得纯净的CHCl3 | |
| B. | 乙醇、乙酸和乙酸乙酯能用饱和Na2CO3溶液鉴别 | |
| C. | C3H6O2有3种同分异构体,它们均能与钠反应放出氢气 | |
| D. | 人体内的蛋白质分解,最终生成二氧化碳和水排出体外 |
2.三氯化硼(BCl3)是一种重要的化工原料.某兴趣小组拟选用下列装置(装置可重复使用),用氯气和硼制备BCl3(已知BCl3的沸点为12.5℃,熔点为-107.3℃;遇水剧烈反应生成硼酸和盐酸).

(1)装置A中反应的离子方程式MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O.
(2)上述装置连接顺序为AACFBDECACFBDEF.
(3)装置A中a管的作用是导气.装置B中饱和食盐水的作用吸收氯气中的氯化氢气体.
(4)已知:硼酸(H3BO3)是一元弱酸,其钠盐化学式为Na[B(OH)4],则硼酸在水中的电离方程式是H3BO3+H2O?[B(OH)4]-+H+.
(5)实验完成后,该小组同学向F中(溶液含有NaClO、NaCl、NaOH)滴加品红溶液,发现溶液褪色,现设计对照实验探究溶液褪色的影响因素.
表格中b值为2.0,通过实验得出的结论是氯化钠浓度越大、溶液碱性越强次氯酸钠漂白性越弱.

(1)装置A中反应的离子方程式MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O.
(2)上述装置连接顺序为AACFBDECACFBDEF.
(3)装置A中a管的作用是导气.装置B中饱和食盐水的作用吸收氯气中的氯化氢气体.
(4)已知:硼酸(H3BO3)是一元弱酸,其钠盐化学式为Na[B(OH)4],则硼酸在水中的电离方程式是H3BO3+H2O?[B(OH)4]-+H+.
(5)实验完成后,该小组同学向F中(溶液含有NaClO、NaCl、NaOH)滴加品红溶液,发现溶液褪色,现设计对照实验探究溶液褪色的影响因素.
| 实验序号 | 0.1mol/LNaClO溶液/mL | 0.1mol/LNaCl溶液/mL | 0.mol/LNaOH溶液/mL | H2O/mL | 品红溶液 | 现象 |
| Ⅰ | 4.0 | 2.0 | 0 | 2.0 | 3滴 | 较快褪色 |
| Ⅱ | 4.0 | 4.0 | 0 | 0 | 3滴 | 缓慢褪色 |
| Ⅲ | 4.0 | 0 | 4.0 | 0 | 3滴 | 缓慢褪色 |
| Ⅳ | 4.0 | 0 | 2.0 | b | 3滴 | 较快褪色 |
9.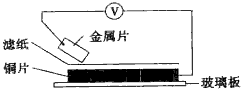 将洁净的金属片甲、乙、丙、丁分别放置在浸有某种盐溶液的滤纸上面并压紧(如图所示).在每次实验时,记录电压指针的移动方向和电压表的读数如表
将洁净的金属片甲、乙、丙、丁分别放置在浸有某种盐溶液的滤纸上面并压紧(如图所示).在每次实验时,记录电压指针的移动方向和电压表的读数如表
已知构成两电极的金属其金属活泼性相差越大,电压表的读数越大.依据记录数据判断,下列结论中正确的是( )
 将洁净的金属片甲、乙、丙、丁分别放置在浸有某种盐溶液的滤纸上面并压紧(如图所示).在每次实验时,记录电压指针的移动方向和电压表的读数如表
将洁净的金属片甲、乙、丙、丁分别放置在浸有某种盐溶液的滤纸上面并压紧(如图所示).在每次实验时,记录电压指针的移动方向和电压表的读数如表 | 金属 | 电子流动方向 | 电压 |
| 甲 | 甲→Cu | +0.78 |
| 乙 | Cu→乙 | +0.15 |
| 丙 | 丙→Cu | +1.35 |
| 丁 | 丁→Cu | +0.30 |
| A. | 在四种金属中乙的还原性最强 | |
| B. | 金属乙能从硫酸铜溶液中置换出铜 | |
| C. | 甲、丁若形成原电池时,甲为负极 | |
| D. | 甲、乙形成合金在空气中,乙先被腐蚀 |