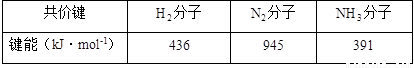题目内容
| 共价键 | H2分子 | N2分子 | NH3分子 |
| 键能(kJ?mol-1) | 436 | 945 | 391 |
(2)在298K时,取1mol氮气和3mol氢气放入一密闭容器中,在催化剂存在下进行反应.理论上放出或吸收的热量为Q1,则Q1为
(2)反应物与生成物的键能差即为热量Q1.
| ||
| 高温高压 |
3×436>0,所以该反应是放热反应,故答案为:放热.
(2)Q1=生成物的键能-反应物的键能=2×3×391KJ-945KJ-3×436=93kJ,
故答案为:93kJ.

 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案在1×105Pa和298K时,将拆开1mol共价键所需要的能量称为键能(kJ·mol-1)。下面是一些共价键的键能:
|
共价键 |
H-H |
N≡N |
N-H |
|
键能(kJ·mol-1) |
436 |
945 |
391 |
(1)根据上表中的数据判断工业合成氨的反应:N2+3H2 2NH3是___________(填“吸热”或“放热”)反应;
2NH3是___________(填“吸热”或“放热”)反应;
(2)在298K时,取1mol氮气和3mol氢气放入一密闭容器中,在催化剂存在下进行反应,若氮气和氢气完全反应,理论上放出或吸收的热量为Q1,则Q1为__________;
(3)实际生产中,放出或吸收的热量为Q2,Q1与Q2比较,正确的是 ( )
A. Q1>Q2 B. Q1<Q2 C. Q1=Q2
如此选择的理由_________________________________________________;
⑷.哈伯因发明了由氮气和氢气合成氨气的方法而获得1918年诺贝尔化学奖。现向一密闭容器中充人1mol N2和3mol H2,在一定条件下使该反应发生:N2+3H2 2NH3。下列有关说法正确的是_______________________.
2NH3。下列有关说法正确的是_______________________.
A.达到化学平衡时,正反应和逆反应的速率都为零。
B.当符合:3u正(N2)=u正(H2)时,反应达到平衡状态。
C.达到化学平衡时,单位时间消耗amolN2,同时生成3amolH2
D.反应达到平衡状态,最多可生成氨2 mol。
E. 工业合成氨,我们希望提高反应物的转化率并加快反应速率。
F.氨分子内形成氢键,使氨的沸点升高.
G.氮分子的分子间作用力大,使氮分子化学性质很稳定.
H.氢能源属于化石能源.