题目内容
2.下列化学用语表达正确的是( )| A. | 氮气的电子式  | B. | 乙烯的结构简式 CH2CH2 | ||
| C. | CO2的结构式 O=O=C | D. | 苯分子的比例模型 |
分析 A.N原子最外层达到8电子稳定结构,漏掉了N原子的1对未成键电子对;
B.乙烯的结构简式中漏掉了碳碳双键;
C.二氧化碳分子中含有两个碳氧双键,中心原子为C原子;
D.苯分子中,碳原子原子半径大于氢原子,为平面结构.
解答 解:A.氮气分子中含有氮氮三键,N原子最外层满足8电子稳定结构,其正确的电子式为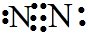 ,故A错误;
,故A错误;
B.乙烯分子中含有1个碳碳双键,其正确的结构简式为CH2=CH2,故B错误;
C.CO2为共价化合物,其分子中含有2个碳氧双键,其正确的结构式为O=C=O,故C错误;
D.苯分子为平面结构,其比例模型为 ,故D正确;
,故D正确;
故选D.
点评 本题考查常见化学用语的表示方法,题目难度不大,涉及电子式、结构简式、比例模型、结构式等知识,明确常见化学用语达到书写原则为解答关键,试题侧重考查学生的规范答题能力.

练习册系列答案
相关题目
3.化学与生活密切相关,下列说法正确的是( )
| A. | 漂白粉长期放置在空气中会被空气中的氧气氧化而变质 | |
| B. | 河水中有许多杂质和有害细菌,加入K2FeO4可以消毒杀菌除杂 | |
| C. | 辽宁舰上用于舰载机降落拦阻索的特种钢缆,属于新型无机非金属材料 | |
| D. | 利用加热的方法杀死人体内感染的埃博拉病毒 |
10.少量铁粉与100mL 0.01mol•L-1的稀盐酸反应,反应速率太慢.为了加快此反应速率而不改变H2的产量,可以使用如下方法中的( )
| A. | 升高温度(不考虑盐酸挥发) | B. | 改用10 mL 0.1 mol/L硝酸 | ||
| C. | 加入NaCl溶液 | D. | 滴入几滴硫酸铜溶液 |
17.下列实验操作能达到目的是( )
| 实验目的 | 实验操作 | |
| A | 制备Fe(OH)3胶体 | 将NaOH浓溶液滴加到饱和FeCl3溶液中 |
| B | 由MgCl2溶液制备无水MgCl2 | 将MgCl2溶液直接加热蒸干 |
| C | 除去乙醇中混有的少量H2O | 加入生石灰,蒸馏 |
| D | 除去乙烷中混有的少量乙烯 | 将混合气体通过酸性高锰酸钾溶液,洗气 |
| A. | A | B. | B | C. | C | D. | D |
7.用下列装置进行实验,能达到相应实验目的是( )
| A. |  可用于吸收多余的NO | |
| B. |  可用于检验SO2的漂白性 | |
| C. |  可用于比较Fe与Cu的金属活动性强弱 | |
| D. |  可用于测定CO2的生成速率 |
14.“绿色化学”对化学反应提出了“原子经济”(原子节约)的新概念及要求,理想原子经济反应是原料中的原子全部转化成所需要的产物,不产生副产物,实现零排放.下列反应类型一定符合这一要求的是( )
①取代反应
②加成反应
③氧化反应
④加聚反应
⑤酯化反应.
①取代反应
②加成反应
③氧化反应
④加聚反应
⑤酯化反应.
| A. | ①② | B. | ①④ | C. | ②④ | D. | ③⑤ |
11.下列化学反应在理论上可设计成原电池的是( )
| A. | CaCO3+2HCl=CaCl2+H2O+CO2↑ | B. | Cu+2AgNO3=2Ag+Cu(NO3)2 | ||
| C. | CaO+H2O=Ca(OH)2 | D. | 3NaOH+FeCl3=3NaCl+Fe(OH)3↓ |
13. 2011年,麻省理工学院科研团队研发出一种人造树叶,它将一片半导体材料夹在两层特殊的催化剂的中间.若将人造树叶整体浸泡在溶液中,当光照在人造树叶上,就会分解水生成H2和O2,结构如图所示.下列有关人造树叶说法正确的是( )
2011年,麻省理工学院科研团队研发出一种人造树叶,它将一片半导体材料夹在两层特殊的催化剂的中间.若将人造树叶整体浸泡在溶液中,当光照在人造树叶上,就会分解水生成H2和O2,结构如图所示.下列有关人造树叶说法正确的是( )
 2011年,麻省理工学院科研团队研发出一种人造树叶,它将一片半导体材料夹在两层特殊的催化剂的中间.若将人造树叶整体浸泡在溶液中,当光照在人造树叶上,就会分解水生成H2和O2,结构如图所示.下列有关人造树叶说法正确的是( )
2011年,麻省理工学院科研团队研发出一种人造树叶,它将一片半导体材料夹在两层特殊的催化剂的中间.若将人造树叶整体浸泡在溶液中,当光照在人造树叶上,就会分解水生成H2和O2,结构如图所示.下列有关人造树叶说法正确的是( )| A. | 该装置最终将太阳能转变为电能 | |
| B. | Ni、Mo、Zn基催化剂极为阳极,发生氧化反应 | |
| C. | 可以将人造树叶浸泡在碱性溶液中 | |
| D. | 钴基催化剂上发生反应:2H2O-4e-=4H++O2↑ |