题目内容
17.实验室制取氯气反应为:MnO2+4HCl(浓) $\frac{\underline{\;△\;}}{\;}$MnCl2+Cl2↑+2H2O,现在用下列两种方法制取氯气:①用含HCl 146g的浓盐酸与足量的MnO2 反应;②用87g MnO2与足量浓盐酸反应.所得的氯气( )| A. | ①比②多 | B. | ②比①多 | C. | 一样多 | D. | 无法比较 |
分析 ①中n(HCl)=$\frac{146g}{36.5g/mol}$=4mol,与足量的MnO2 反应,HCl完全反应;
②中n(MnO2)=$\frac{87g}{87g/mol}$=1mol,浓盐酸足量,但随反应的进行,浓盐酸变为稀盐酸,稀盐酸与二氧化锰不反应,以此来解答.
解答 解:①中n(HCl)=$\frac{146g}{36.5g/mol}$=4mol,与足量的MnO2 反应,HCl完全反应,结合MnO2+4HCl(浓) $\frac{\underline{\;△\;}}{\;}$MnCl2+Cl2↑+2H2O可知,生成氯气为1mol;
②中n(MnO2)=$\frac{87g}{87g/mol}$=1mol,浓盐酸足量,但随反应的进行,浓盐酸变为稀盐酸,稀盐酸与二氧化锰不反应,结合MnO2+4HCl(浓) $\frac{\underline{\;△\;}}{\;}$MnCl2+Cl2↑+2H2O可知,生成氯气小于1mol,
则生成氯气为①比②多,
故选A.
点评 本题考查氧化还原反应的计算,为高频考点,把握反应中物质的量关系为解答的关键,侧重分析与计算能力的考查,注意稀盐酸与二氧化锰不反应,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
20.对下列现象或事实的解释不正确的是( )
| 选项 | 现象或事实 | 解释 |
| A | 铝箔在酒精灯上加热,熔化后的液态铝不滴落 | 高熔点的氧化铝薄膜兜在铝的外面,阻止了液态铝滴落 |
| B | 铁放在冷的浓硝酸中不溶解,无红棕色气体生成 | 铁遇浓硝酸钝化,表面形成致密的氧化膜,阻止内部铁继续与硝酸反应 |
| C | 漂白粉在空气中久置变质 | 漂白粉中的CaCl2与空气中的CO2反应生成CaCO3 |
| D | 将新制氯水滴到蓝色石蕊试纸上,试纸先变红后褪色 | 新制氯水中的H+使石蕊试纸先变红,HClO的强氧化性使石蕊试纸褪色 |
| A. | A | B. | B | C. | C | D. | D |
1.下列说法不正确的是( )
| A. | 二氧化硫和氯气都能使品红溶液褪色 | |
| B. | 漂白粉暴露在空气中久置会变质 | |
| C. | 在加热条件下,镁能在二氧化碳气体中燃烧 | |
| D. | 氯水中真正起漂白、杀菌、消毒作用的微粒是其中含有的Cl2分子 |
5.铝制品具有较强的抗腐蚀性,主要是因为( )
| A. | 铝的化学性质稳定 | |
| B. | 铝在常温时与氧气不反应 | |
| C. | 铝具有金属性,也具有非金属性 | |
| D. | 铝与氧气反应生成一层致密的氧化物薄膜 |
12.实验室里可按如图所示的装置干燥、储存气体 R,多余的气体可用水吸收,则 R是( )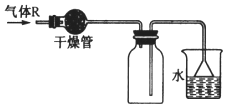

| A. | NO2 | B. | HCl | C. | SO2 | D. | NH3 |
9.化学与生活密切相关,下列说法错误的是( )
| A. | 食盐中加有碘,用其配成的溶液遇淀粉变蓝 | |
| B. | 厕所清洁剂、食用醋、肥皂水、厨房清洁剂四种溶液的pH逐渐增大 | |
| C. | 使用氯气自来水消毒时,氯气会与自来水中的有机物反应,生成的有机氯化物可能对人有害 | |
| D. | 硅胶、生石灰、氯化钙等都是食品包装袋中常用的干燥剂. |
6.下列关于氯离子的表示方法,错误的是( )
| A. | Cl- | B. | 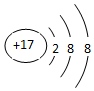 | C. | 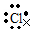 | D. | 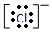 |
7.Y元素的阳离子和X元素的阴离子具有与氩原子相同的电子层结构,下列叙述正确的是( )
| A. | Y的原子序数比X的大 | B. | Y的离子半径比X的离子大 | ||
| C. | Y原子的最外层电子数比X的大 | D. | Y元素的最高正价比X的大 |
 作为高中生,学会利用我们课堂上学到的知识来解决生活中的一些问题,是我们学习的重要目的之一.某中学的化学实验兴趣小组,一行四人,利用实验室老师提供的基本仪器和药品,自行购置了鸡蛋,食醋等生活用品,进行了如下探究.
作为高中生,学会利用我们课堂上学到的知识来解决生活中的一些问题,是我们学习的重要目的之一.某中学的化学实验兴趣小组,一行四人,利用实验室老师提供的基本仪器和药品,自行购置了鸡蛋,食醋等生活用品,进行了如下探究.