题目内容
7.下列有关说法正确的是( )| A. | 明矾既可用作净水剂,也可用作消毒剂 | |
| B. | 小苏打、氢氧化铝都可用于治疗胃酸过多 | |
| C. | 煤的干馏、石油的分馏都属于化学变化 | |
| D. | 已知PM2.5是指大气中直径小于或等于2.5微米(1微米=1000纳米)的颗粒物,则PM2.5在空气中能形成胶体 |
分析 A.明矾不具有强氧化性,不能杀菌消毒;
B.小苏打、氢氧化铝的碱性均较弱,均与盐酸反应;
C.石油的分馏与沸点有关;
D.PM2.5是指大气中直径小于或等于2.5微米,而分散质的直径在1~100nm为胶体分散系.
解答 解:A.明矾不具有强氧化性,不能杀菌消毒,可用作净水剂,故A错误;
B.小苏打、氢氧化铝的碱性均较弱,均与盐酸反应,则小苏打、氢氧化铝都可用于治疗胃酸过多,故B正确;
C.石油的分馏与沸点有关,为物理变化,而煤的干馏生成煤焦油等属于化学变化,故C错误;
D.PM2.5是指大气中直径小于或等于2.5微米颗粒物,2.5微米为2500nm,而分散质的直径在1~100nm为胶体分散系,则PM2.5在空气中不一定形成胶体,故D错误;
故选B.
点评 本题考查物质的性质及应用,为高频考点,把握物质的性质、发生的反应、性质与用途为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大.

练习册系列答案
相关题目
13.下列离子方程式正确的是( )
| A. | 向氢氧化亚铁中加入足量稀硝酸:Fe(OH)2+2H+═Fe2++2H2O | |
| B. | 向 NaClO 溶液中通入过量SO2气体:ClO-+H2O+SO2═HClO+HSO3- | |
| C. | 向偏铝酸钠溶液中加入碳酸氢钠:AlO2-+3HCO3-═Al(OH)3↓+3CO2↑ | |
| D. | 向NH4HCO3溶液中加入过量NaOH溶液:NH4++HCO3-+2OH-═NH3•H2O+H2O+CO32- |
2.某学生探究0.25mol/LAl2(SO4)3溶液与0.5mol/LNa2CO3溶液的反应,实验如表.
下列分析不正确的是( )
| 实验1 | 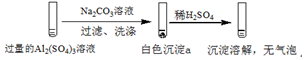 |
| 实验2 | 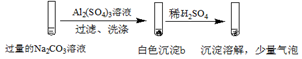 |
| A. | 实验1中,白色沉淀a是Al(OH)3 | |
| B. | 实验2中,白色沉淀b含有CO32- | |
| C. | 实验1、2中,白色沉淀成分不同的原因与混合后溶液的pH无关 | |
| D. | 检验白色沉淀a、b是否洗涤干净,均可用盐酸酸化的BaCl2溶液 |
12.据报导,我国已研制出“可充室温钠一二氧化碳电池”,电极材料为钠金属片和碳纳米管,电解液为高氯酸钠一四甘醇二甲醚,电池总反应为:4Na+3CO2 $?_{充电}^{放电}$2Na2CO3+C,生成固体Na2CO3沉积在碳纳米管上.下列叙述不正确的是( )
| A. | 放电时钠金属片发生氧化反应 | |
| B. | 充电时碳纳米管接直流电源的正极 | |
| C. | 放电时每消耗3molCO2,转移12 mol电子 | |
| D. | 充电时的阳极反应为C+2Na2CO3-4e-=3CO2↑+4Na+ |
19.下列关于实验室制取乙酸丁酯的叙述,正确的是( )
| A. | 使用过量的乙酸 | B. | 采用边反应边蒸馏的方法 | ||
| C. | 反应采用水浴加热 | D. | 用氢氧化钠溶液提纯乙酸丁酯 |
16.用NA表示阿伏加德罗常数的值.下列叙述中正确的是( O-16 N-16 )( )
| A. | 1 mol甲基(CH3-)所含的电子数分别为10NA | |
| B. | 标准状况下,22.4 L四氯化碳中含有C-Cl键的数目为4NA | |
| C. | 常温常压下,1 mol分子式为C2H6O的有机物中,含有C-O键的数目为NA | |
| D. | 46g 由NO2和N2O4组成的混合气体中,含有的原子总数为3NA |
17.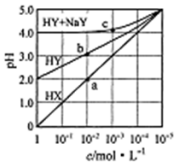 常溫下,浓度均为1.0mol/L的HX溶液、HY溶液、HY和 NaY的混合溶液,分别加水稀释,稀释后溶液的pH随浓度的变化如图所示,下列叙述正确的是( )
常溫下,浓度均为1.0mol/L的HX溶液、HY溶液、HY和 NaY的混合溶液,分别加水稀释,稀释后溶液的pH随浓度的变化如图所示,下列叙述正确的是( )
 常溫下,浓度均为1.0mol/L的HX溶液、HY溶液、HY和 NaY的混合溶液,分别加水稀释,稀释后溶液的pH随浓度的变化如图所示,下列叙述正确的是( )
常溫下,浓度均为1.0mol/L的HX溶液、HY溶液、HY和 NaY的混合溶液,分别加水稀释,稀释后溶液的pH随浓度的变化如图所示,下列叙述正确的是( )| A. | HX是强酸,溶液每稀释10倍,pH始终增大1 | |
| B. | 常温下HY的电离常数为1.0×10-4 | |
| C. | 溶液中水的电离程度:a点大于b点 | |
| D. | c 点溶液中:c(Na+)>c(Y-)>c(HY)c(H+)>c(OH-) |