题目内容
11.已知:2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ•mol-1
CH4(g)+2O2(g)═CO2(g)+2H2O(1)△H=-890.31kJ•mol-1
下列说法正确的是( )
| A. | 根据上述热化学方程式可以确定H2、CH4的燃烧热 | |
| B. | H2(g)+$\frac{1}{2}$O2(g)═H2O(1)△H=-241.8kJ•mol-1 | |
| C. | CH4(g)+$\frac{3}{2}$O2(g)═CO(g)+2H2O(g)△H>-890.31kJ•mol-1 | |
| D. | 8gCH4完全燃烧释放出的热量为445.155kJ |
分析 A、氢气生成稳定的氧化物液态水;
B、不液态转化气态的热量变化;
C、不完全燃烧放出的热量少,变成气态水放出的热量少;
D、反应物和生成物的状态不知.
解答 解:A、氢气生成稳定的氧化物液态水,所以无法确定氢气的燃烧热,故A错误;
B、不液态转化气态的热量变化,而气态水变成液水要放出热量,所以H2(g)+$\frac{1}{2}$O2(g)═H2O(1)△H<-241.8kJ•mol-1,故B错误;
C、不完全燃烧放出的热量少,变成气态水放出的热量少,所以CH4(g)+$\frac{3}{2}$O2(g)═CO(g)+2H2O(g)△H>-890.31kJ•mol-1,故C正确;
D、反应物和生成物的状态不知,所以无法判断能量的变化,故D错误;
故选C.
点评 本题考查了热化学方程式和燃烧热的计算的应用,热化学方程式的计算分析,题目难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
1.下列离子方程式正确的是( )
| A. | 向苏打溶液中滴加少量的稀盐酸:CO32-+2H+═H2O+CO2↑ | |
| B. | 向MgCl2溶液中加入一小块钠:2Na+2H2O═2Na++2OH-+H2↑ | |
| C. | 向AlCl3溶液中加入过量的氨水:Al3++3NH3•H2O═Al(OH)3↓+3NH4+ | |
| D. | 用FeCl3溶液腐蚀印刷电路板上铜箔:Fe3++Cu═Fe2++Cu |
2.下列关于HClO的说法不正确的是( )
| A. | HClO是强酸 | B. | HClO不稳定 | ||
| C. | HClO是强氧化性酸 | D. | HClO能杀菌消毒 |
19.下列说法正确的是( )
| A. | 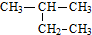 与 与 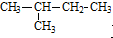 互为同分异构体 互为同分异构体 | |
| B. | 红磷与白磷互为同素异形体 | |
| C. | CH3CH2OH与HOCH2CH2CH2OH互为同系物 | |
| D. | 35Cl与37Cl为同一种核素 |
16.下列各组离子在pH=1的溶液中,因发生氧化还原反应而不能大量共存的是( )
| A. | Na+、K+、CO32-、NO3- | B. | NH4+、Na+、SO42-、S2- | ||
| C. | Al3+、Na+、NO3-、I- | D. | CH3COO-、Cl-、Na+、NH4+ |
7.氢能是一种洁净的可再生能源,制备和储存氢气是氢能开发的两个关键环节.
Ⅰ氢气的制取
(1)水是制取氢气的常见原料,下列说法正确的是AB(填序号).
A.H3O+的空间构型为三角锥形
B.水的沸点比硫化氢高
C.冰晶体中,1mol水分子可形成4mol氢键
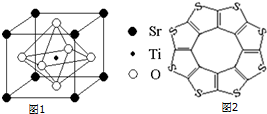
(2)科研人员研究出以钛酸锶为电极的光化学电池,用紫外线照射钛酸锶电极,使水分解产生氢气.已知钛酸锶晶胞结构如图1,则其化学式为SrTiO3.
Ⅱ氢气的存储
(3)Ti(BH4)2是一种储氢材料.
①Ti原子在基态时的核外电子排布式是1s22s22p63s23p63d24s2或[Ar]3d24s2.
②Ti(BH4)2可由TiCl4和LiBH4反应制得,TiCl4 熔点-25.0℃,沸点136.94℃,常温下是无色液体,则TiCl4晶体类型为分子晶体.
(4)最近尼赫鲁先进科学研究中心借助ADF软件对一种新型环烯类储氢材料(C16S8)进行研究,从理论角度证明这种分子中的原子都处于同一平面上(结构如图2所示),每个平面上下两侧最多可储存10个H2分子.
①元素电负性大小关系是:C<S(填“>”、“=”或“<”).
②分子中C原子的杂化轨道类型为sp2.
③有关键长数据如下:
从表中数据可以看出,C16S8中碳硫键键长介于C-S与C═S之间,原因可能是:分子中的C与S原子之间有π键或分子中的碳硫键具有一定程度的双键性质.
④C16S8与H2微粒间的作用力是范德华力.
Ⅰ氢气的制取
(1)水是制取氢气的常见原料,下列说法正确的是AB(填序号).
A.H3O+的空间构型为三角锥形
B.水的沸点比硫化氢高
C.冰晶体中,1mol水分子可形成4mol氢键
(2)科研人员研究出以钛酸锶为电极的光化学电池,用紫外线照射钛酸锶电极,使水分解产生氢气.已知钛酸锶晶胞结构如图1,则其化学式为SrTiO3.

Ⅱ氢气的存储
(3)Ti(BH4)2是一种储氢材料.
①Ti原子在基态时的核外电子排布式是1s22s22p63s23p63d24s2或[Ar]3d24s2.
②Ti(BH4)2可由TiCl4和LiBH4反应制得,TiCl4 熔点-25.0℃,沸点136.94℃,常温下是无色液体,则TiCl4晶体类型为分子晶体.
(4)最近尼赫鲁先进科学研究中心借助ADF软件对一种新型环烯类储氢材料(C16S8)进行研究,从理论角度证明这种分子中的原子都处于同一平面上(结构如图2所示),每个平面上下两侧最多可储存10个H2分子.
①元素电负性大小关系是:C<S(填“>”、“=”或“<”).
②分子中C原子的杂化轨道类型为sp2.
③有关键长数据如下:
| C-S | C═S | C16S8中碳硫键 | |
| 键长/pm | 181 | 155 | 176 |
④C16S8与H2微粒间的作用力是范德华力.
8.下列实验操作和数据记录都正确的是( )
| A. | 用托盘天平称量时,将NaOH固体放在左盘内的纸上,称得质量为10.2 g | |
| B. | 用25 mL碱式滴定管量取高锰酸钾溶液,体积为16.60 mL | |
| C. | 用广泛pH试纸测稀盐酸的pH=3.2 | |
| D. | 用10 mL量筒量取NaCl溶液,体积为9.2 mL |
 .
.