题目内容
向一定量下列物质的溶液中逐滴加入氢氧化钠溶液,先生成白色沉淀,后沉淀逐渐溶解.这种物质是( )
| A、硫酸镁 | B、偏铝酸钠 |
| C、氯化铝 | D、氯化铁 |
考点:两性氧化物和两性氢氧化物
专题:
分析:A.硫酸镁与氢氧化钠反应生成氢氧化镁白色沉淀,氢氧化镁不能溶于氢氧化钠溶液;
B.偏铝酸钠与氢氧化钠不反应;
C.氯化铝与氢氧化钠反应生成氢氧化铝白色沉淀,氢氧化钠过量,溶解氢氧化铝,白色沉淀减小至消失;
D.氯化铁与氢氧化钠反应生成氢氧化铁红褐色沉淀.
B.偏铝酸钠与氢氧化钠不反应;
C.氯化铝与氢氧化钠反应生成氢氧化铝白色沉淀,氢氧化钠过量,溶解氢氧化铝,白色沉淀减小至消失;
D.氯化铁与氢氧化钠反应生成氢氧化铁红褐色沉淀.
解答:
解:A.硫酸镁与氢氧化钠反应生成氢氧化镁白色沉淀,氢氧化镁不能溶于氢氧化钠溶液,故A不符合;
B.偏铝酸钠与氢氧化钠不反应,故B不符合;
C.首先发生反应AlCl3+3NaOH═Al(OH)3↓+3NaCl,生成白色沉淀,氢氧化钠过量,Al(OH)3溶于NaOH溶液,反应式为Al(OH)3+NaOH═NaAlO2+2H2O,白色沉淀逐渐溶解,故C符合;
D.氯化铁与氢氧化钠反应生成氢氧化铁红褐色沉淀,氢氧化钠过量,氢氧化铁不溶解,故D不符合;
故选C.
B.偏铝酸钠与氢氧化钠不反应,故B不符合;
C.首先发生反应AlCl3+3NaOH═Al(OH)3↓+3NaCl,生成白色沉淀,氢氧化钠过量,Al(OH)3溶于NaOH溶液,反应式为Al(OH)3+NaOH═NaAlO2+2H2O,白色沉淀逐渐溶解,故C符合;
D.氯化铁与氢氧化钠反应生成氢氧化铁红褐色沉淀,氢氧化钠过量,氢氧化铁不溶解,故D不符合;
故选C.
点评:本题考查元素化合物的性质,难度不大,注意掌握理解与反应物的量、先后顺序及反应条件有关的反应.

练习册系列答案
 华东师大版一课一练系列答案
华东师大版一课一练系列答案
相关题目
每年的6月26日是国际禁毒日.以下是四种毒品的结构简式,下列有关说法正确的是( )
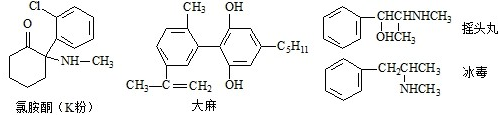

| A、四种毒品中都含有苯环,都属于芳香烃 |
| B、摇头丸经消去、加成反应可制得冰毒 |
| C、1mol大麻与溴水反应最多消耗4mol Br2 |
| D、氯胺酮分子中环上所有碳原子可能共平面 |
下列各组中都是酸性食物的是( )
| A、猪肉 大米 苹果 花生 |
| B、豆腐 鸡肉 面包 小麦 |
| C、玉米 海带 西瓜 面粉 |
| D、大麦 玉米 牛肉 蛋黄 |
糖类、油脂、蛋白质是人类基本营养物质,关于糖类、油脂、蛋白质的说法正确的是( )
| A、单糖可以发生水解反应 |
| B、油脂皂化是取代反应,硬化也是取代反应 |
| C、氨基酸、多肽、蛋白质都具有两性 |
| D、饱和Na2SO4、CuSO4溶液均可用于蛋白质的盐析 |
化学与工农业生产和人类生活密切相关.下列说法中正确的是( )
| A、铜矿石在细菌作用下可直接转化为单质铜,这个过程叫生物炼铜 |
| B、用纯碱制玻璃、用铁矿石炼铁、用氨制碳酸铵都会产生温室气体 |
| C、海轮外壳上镶入锌块,可减缓船体的腐蚀,该方法叫牺牲阳极的阴极保护法 |
| D、酸雨就是pH<7的雨水,主要是由大气中的SO2、NO2等造成的 |
下列各组溶液中,离子一定能大量共存的是( )
| A、强碱性溶液中:Na+、K+、SO42-、AlO2- |
| B、强酸性溶液中:K+、Fe3+、Cl-、SCN- |
| C、某无色溶液中:H+、Fe2+、NH4+、NO3- |
| D、与铝反应生成H2的溶液中:Na+、Mg2+、Cl-、CO32- |
下列关于乙炔制取的说法不正确的是 ( )
| A、用饱和食盐水代替水反应是为了控制反应速率 |
| B、此反应需要加热 |
| C、可用硫酸铜溶液除去杂质气体 |
| D、反应中不需加碎瓷片作沸石 |
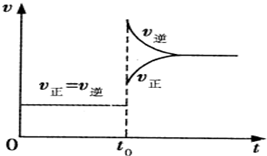 往一体积不变的密闭容器中充入H2和I2,发生反应H2(g)+I2(g)?2HI(g);△H<0,当达到平衡后,t0时若保持混合气体总物质的量不变而改变某一反应条件,使容器内压强增大(如图所示),下列说法正确的是.( )
往一体积不变的密闭容器中充入H2和I2,发生反应H2(g)+I2(g)?2HI(g);△H<0,当达到平衡后,t0时若保持混合气体总物质的量不变而改变某一反应条件,使容器内压强增大(如图所示),下列说法正确的是.( )| A、容器内气体颜色变深,平均相对分子质量不变 |
| B、平衡不移动,混合气体密度增大 |
| C、H2转化率增大,HI平衡浓度减小 |
| D、t0时减小体积或升高体系温度 |
下列离子化合物中阳离子半径最小的是( )
| A、KCl |
| B、NaF |
| C、HF |
| D、Cs2S |