题目内容
向100mLFeBr2溶液中通入标准状况下的C12 3.36 L,C12全部被还原,测得溶液中c(Br–)=c(C1–),则原FeBr2溶液的物质的量浓度是
- A.2mol/L
- B.3 mol/ L
- C.1.5 mol/ L
- D.0.75mol/L
A
设原溶液中FeBr2的物质的量为n mol
氯气的物质的量为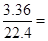 0.15mol,在反应中得电子0.3mol,形成的溶液中的Cl—的物质的量为0.3 mol,没有反应的Br—的物质的量也为0.3mol
0.15mol,在反应中得电子0.3mol,形成的溶液中的Cl—的物质的量为0.3 mol,没有反应的Br—的物质的量也为0.3mol
则参加反应被氧化的Fe2+、Br-的物质的量为n mol、(2n—0.3)mol,故两离子失电子总数为(n+2n—0.3)mol,由得失电子守恒知:3n—0.3=0.3,求得n=0.2
故原FeBr2溶液的物质的量浓度为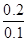 =2mol/L
=2mol/L
设原溶液中FeBr2的物质的量为n mol
氯气的物质的量为
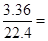 0.15mol,在反应中得电子0.3mol,形成的溶液中的Cl—的物质的量为0.3 mol,没有反应的Br—的物质的量也为0.3mol
0.15mol,在反应中得电子0.3mol,形成的溶液中的Cl—的物质的量为0.3 mol,没有反应的Br—的物质的量也为0.3mol则参加反应被氧化的Fe2+、Br-的物质的量为n mol、(2n—0.3)mol,故两离子失电子总数为(n+2n—0.3)mol,由得失电子守恒知:3n—0.3=0.3,求得n=0.2
故原FeBr2溶液的物质的量浓度为
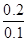 =2mol/L
=2mol/L 
练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目