题目内容
反应3A(g)+B(g)?2C(g)+2D(g),在不同情况下测得反应速率如下,其中反应速率最快的是( )
| A、v (A)=0.15 mol?L-1?s-1 |
| B、v (B)=0.3 mol?L-1?s-1 |
| C、v (C)=0.5 mol?L-1?s-1 |
| D、v(D)=0.4 mol?L-1?s-1 |
考点:化学反应速率和化学计量数的关系
专题:化学反应速率专题
分析:不同物质表示的速率之比等于其化学计量数之比,故不同物质表示的速率与其化学计量数的比值越大,表示的反应速率越快,注意保持单位一致.
解答:
解:A.
=0.05 mol?L-1?s-1;
B.
=0.1 mol?L-1?s-1;
C.
=0.25 mol?L-1?s-1;
D.
=0.2 mol?L-1?s-1;
故反应速率v(C)>v(D)>v(B)>v(A),
故选C.
| v(A) |
| 3 |
B.
| v(B) |
| 3 |
C.
| v(C) |
| 2 |
D.
| v(D) |
| 2 |
故反应速率v(C)>v(D)>v(B)>v(A),
故选C.
点评:本题考查化学反应速率快慢比较,题目基础性强,贴近教材,利用比值法可以迅速判断,也可以转化为同一物质表示的速率比较.

练习册系列答案
 天天向上口算本系列答案
天天向上口算本系列答案
相关题目
高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压.高铁电池的总反应为3Zn+2K2FeO4+8H2O
3Zn(OH)2+2Fe(OH)3+4KOH,关于该电池的说法正确的是( )
| 放电 |
| 充电 |
| A、放电时,Zn作负极,发生还原反应 |
| B、放电时,K2FeO4附近溶液pH减小 |
| C、充电时,锌极附近溶液pH减小 |
| D、充电时,阳极电极反应为:Fe(OH)3-3e-+5OH-═FeO42-+4H2O |
下列有关金属认识正确的是( )
| A、金属单质均只能作还原剂,离子只能作氧化剂 |
| B、活动性强的金属均可从盐溶液中置换出活动性弱的金属 |
| C、碱性氧化物都是金属氧化物 |
| D、合金均比纯金属的熔点高、硬度大 |
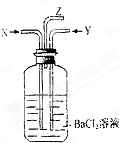 碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图所示),下列说法正确的是( )
碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图所示),下列说法正确的是( )| A、洗气瓶中产生的沉淀是BaCO3 |
| B、在Z导管出来的气体中无CO2 |
| C、洗气瓶中产生的沉淀是BaSO3 |
| D、在Z导管口有红棕色气体出现 |
 科学家最近研制出可望成为高效火箭推进剂的 N(NO2)3(如图所示).已知该分子中N-N-N键角都是108.1°.下列有关N(NO2)3的说法正确的是( )
科学家最近研制出可望成为高效火箭推进剂的 N(NO2)3(如图所示).已知该分子中N-N-N键角都是108.1°.下列有关N(NO2)3的说法正确的是( )| A、分子中N、O原子间形成的共价键是非极性键 |
| B、分子中四个氮原子共平面 |
| C、该物质既有氧化性又有还原性 |
| D、分子中四个氮原子围成一个空间正四面体 |