题目内容
1.碳酸镁晶体是一种新型吸波隐形材料中的增强剂.实验一:合成碳酸镁晶体的步骤:
①配制一定浓度的MgSO4溶液和NH4HCO3溶液;
②量取一定量的NH4 HCO3溶液于容器中,搅拌并逐滴加入MgSO4溶液,控制温度50℃,反应一段时间;
③用氨水调节溶液pH至9.5,放置一段时间后,过滤、洗涤、干燥得碳酸镁晶体产品.
称取3.000g MgSO4样品配制250mL溶液流程如图所示:
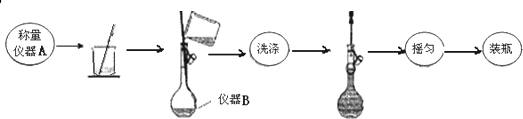
回答下列问题:
(1)写出实验仪器名称:A电子天平;B250mL容量瓶.配制溶液过程中定容后的“摇匀”的实验操作为把容量瓶瓶塞塞紧,用食指顶住瓶塞,用另一只手的手指托住瓶底,把容量瓶上下颠倒摇动多次,使溶液混合均匀.
(2)检验碳酸镁晶体是否洗干净的方法是取最后一次洗涤液少许于试管,加入稀盐酸酸化,再加入几滴氯化钡溶液,若不再产生白色沉淀,则说明沉淀已洗干净.
实验二:测定产品MgCO3•nH2O中的n值(仪器和药品如图所示):

(3)实验二装置的连接顺序为a→e、d→b(按气流方向,用接口字母abcde表示),其中Ⅱ装置的作用是吸收CO2以便测定样品中碳元素的含量.
(4)加热前先通入N2排尽装置Ⅰ中的空气,然后称取装置Ⅱ、Ⅲ的初始质量.进行加热时还需通入N2的作用是将分解生成的气体全部带入装置Ⅱ或Ⅲ中,使其完全吸收,并防止倒吸.
(5)若要准确测定n值,至少需要下列所给数据中的b、c(填选项字母),写出相应1种组合情景下,求算n值的数学表达式:n=$\frac{22{m}_{3}}{9{m}_{2}}$.
a.装置Ⅰ反应前后质量差m1 b.装置Ⅱ反应前后质量差m2 c.装置Ⅲ反应前后质量差m3.
分析 (1)称取3.000g MgSO4样品,需要用到电子天平,配制250mL溶液需要250mL容量瓶;
(2)检验沉淀已经洗涤干净的方法是检验洗涤液中是否含有硫酸根离子来检验是否洗净;
(3)实验目的是测定产品MgCO3•nH2O中的n值,需要测量水和二氧化碳的量,将气体通过洗气瓶进行洗气时,应该从长导管一侧通入气体;
(4)为了避免引起实验误差,保证反应产生的气体全部被装置C、D吸收,所以要通入N2排出装置内残留的气体,同时也是为了防止产生倒吸;
(5)若B装置中无残留物,通过装置D吸收的质量为生成水的质量,装置C吸收的是分解生成的二氧化碳的质量,据此计算物质的量得到n值.
解答 解:(1)称取3.000g MgSO4样品,需要用到电子天平,故A为电子天平,配制250mL溶液需要250mL容量瓶,故B为250mL容量瓶,“摇匀”的实验操作为把容量瓶瓶塞塞紧,用食指顶住瓶塞,用另一只手的手指托住瓶底,把容量瓶上下颠倒摇动多次,使溶液混合均匀,
故答案为:电子天平;250mL容量瓶;把容量瓶瓶塞塞紧,用食指顶住瓶塞,用另一只手的手指托住瓶底,把容量瓶上下颠倒摇动多次,使溶液混合均匀;
(2)检验碳酸镁晶体是否洗干净的方法是取最后一次洗涤液少许于试管,加入稀盐酸酸化,再加入几滴氯化钡溶液,若不再产生白色沉淀,则说明沉淀已洗干净,
故答案为:取最后一次洗涤液少许于试管,加入稀盐酸酸化,再加入几滴氯化钡溶液,若不再产生白色沉淀,则说明沉淀已洗干净;
(3)加热装置Ⅰ产生的气体二氧化碳和水蒸气依次通过浓硫酸和氢氧化钠溶液吸收,可以测定二氧化碳和水蒸气的量,故装置连接顺序为a→e、d→b,其中Ⅱ装置为碱性溶液吸收CO2以便测定样品中碳元素的含量,进而计算MgCO3•nH2O中的n值,
故答案为:a→e、d→b;吸收CO2以便测定样品中碳元素的含量;
(4)进行加热时还需通入N2的作用是将分解生成的气体全部带入装置Ⅱ或Ⅲ中,使其完全吸收,减少测定产生的误差,并防止倒吸,
故答案为:将分解生成的气体全部带入装置Ⅱ或Ⅲ中,使其完全吸收,并防止倒吸;
(5)若B装置中无残留物,通过装置D吸收的质量为生成水的质量,装置C吸收的是分解生成的二氧化碳的质量,b.装置C反应前后质量差m2 c.装置D反应前后质量差m3,可以计算,$\frac{{m}_{2}}{44}$:$\frac{{m}_{3}}{18}$=1:n,n=$\frac{22{m}_{3}}{9{m}_{2}}$,
故答案为:b、c;$\frac{22{m}_{3}}{9{m}_{2}}$.
点评 本题考查物质的组成的测定,主要考查对实验装置和实验流程的理解和熟悉实验操作,同时通过计算,确定水分子数.综合性较强,题目难度中等.

 如图是某同学研究铜与浓硫酸的反应装置:
如图是某同学研究铜与浓硫酸的反应装置:完成下列填空:
(1)写出A中发生反应的化学方程式Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+2H2O+SO2↑.
采用可抽动铜丝进行实验的优点是可以控制反应的进行.
(2)反应一段时间后,可观察到B试管中的现象为变红.
(3)从C试管的直立导管中向BaCl2溶液中通入另一种气体,产生白色沉淀,则气体可以是NH3、
Cl2.(要求填一种化合物和一种单质的化学式)
(4)反应完毕,将A中的混合物倒入水中,得到呈酸性的蓝色溶液与少量黑色不溶物,分离出该不溶物的操作是过滤.该黑色不溶物不可能是CuO,理由是CuO会溶于稀硫酸中.
(5)对铜与浓硫酸反应产生的黑色不溶物进行探究,实验装置及现象如下:
| 实验装置 | 实验现象 |
 | 品红褪色 |
②若该黑色不溶物由两种元素组成且在反应前后质量保持不变,推测其化学式为Cu2S.
| A. | 配制氯化铁溶液时需加入少量盐酸 | |
| B. | 金属钠保存在装有煤油的带玻璃塞的广口瓶中 | |
| C. | 保存液溴需用水封,放在带橡皮塞子的棕色细口瓶中 | |
| D. | 用稀硝酸洗去附在试管内壁的银镜 |
| 反应时间min | n(CO)/mol | n(H2O)/mol |
| 0 | 1.20 | 0.60 |
| t1 | 0.80 | |
| t2 | 0.20 |
| A. | 增大压强对正逆反应速率没有影响,平衡不移动 | |
| B. | 保持其他条件不变,起始时向容器中充入0.60 mol CO和1.20 mol H2O(g),达到平衡时n(CO2)=0.40 mol | |
| C. | 保持其他条件不变,向平衡体系中再通入0.20mol H2O(g),与原平衡相比,达到新平衡时CO转化率增大,H2O的体积分数增大 | |
| D. | 由表格中数据得出,t1时刻该反应还未达到平衡 |
| A. | 氢氧化钠、盐酸都为强电解质 | |
| B. | 铁生锈、食物腐败都有氧化反应发生 | |
| C. | 糖类、蛋白质都为高分子化合物 | |
| D. | 一氯甲烷、二氧化碳都是极性分子 |
| A. | 同周期金属元素的化合价越高,元素的金属性越强 | |
| B. | 海轮外壳上附着一些锌块,可以减缓海轮外壳的腐蚀 | |
| C. | 在含有 BaSO4 沉淀的溶液中加入 Na2SO4固体,c(Ba2+) 增大 | |
| D. | 2NO(g)+2CO(g)═N2(g)+2CO2(g) 在常温下能自发进行,则该反应的△H>0 |
| A. | ①②③④ | B. | ②③④① | C. | ④③②① | D. | ②③①④ |


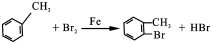 ,F的结构简式
,F的结构简式 .
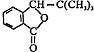
.
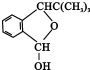 .
.