题目内容
3.写出下列化学反应方程式:(1)乙醇的消去反应:CH3CH2OH$→_{170℃}^{浓硫酸}$C2H4↑+H2O.
(2)苯酚与浓溴水反应:
 .
.(3)硬脂酸甘油酯的皂化反应:
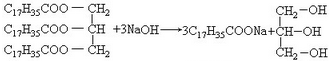 .
.
分析 (1)乙醇发生消去反应生成乙烯和水,断开的碳氧单键和甲基上的碳氢键;
(2)苯酚与浓溴水反应,是苯酚分子中羟基对苯环影响,邻对位氢原子活泼,易于取代;
(3)硬脂酸甘油酯在碱性条件下水解生成硬脂酸盐和甘油.
解答 解:(1)乙醇发生消去反应,断开的碳氧单键和甲基上的碳氢键,反应为:CH3CH2OH$→_{170℃}^{浓硫酸}$C2H4↑+H2O,
故答案为:CH3CH2OH$→_{170℃}^{浓硫酸}$C2H4↑+H2O;
(2)苯酚与浓溴水反应,是苯酚分子中羟基对苯环影响,邻对位氢原子活泼,易于取代反应的化学方程式为 ,
,
故答案为: ;
;
(3)硬脂酸甘油酯在碱性条件下水解的化学方程式为: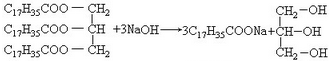 ;
;
故答案为: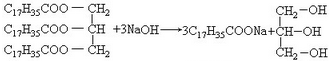 .
.
点评 本题考查了有机物质的性质应用以及反应类型的判断,掌握物质官能团的性质是解题关键.题目较简单.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
9.下列叙述正确的是( )
| A. | NaCl的摩尔质量是58.5 g | |
| B. | 含1 mol NaCl的溶液中约含有6.02×1023个Cl- | |
| C. | 1 mol NaCl的质量是58.5 g•mol-1 | |
| D. | 58.5 g NaCl所含Na+和Cl-共1mol |
11.下列各组中两种气体的分子数一定相等的是( )
| A. | 温度相同、体积相同的O2和N2 | B. | 质量相等、密度不等的N2和C2H4 | ||
| C. | 体积相同、密度相等的CO和N2O | D. | 压强相同、体积相同的O2和H2 |
18.下列有关胶体及其性质的叙述正确的是( )
| A. | Fe(OH)3胶体无色、透明,能发生丁达尔现象 | |
| B. | 水泥厂、冶金厂常用高压电除去烟尘,是因为烟尘微粒带电荷 | |
| C. | 胶体与其它分散系的本质区别是胶体有丁达尔效应,而其它分散系却没有 | |
| D. | 纳米材料 微粒直径从几纳米到几十纳米(1nm=10-9m),因此纳米材料属于胶体 |
8.下列关于氧化性、还原性的判断正确的是( )
| A. | B的阳离子的氧化性比A的阳离子强,则A元素的金属性不一定比B元素强 | |
| B. | 发生氧化还原反应时,A原子失去的电子比B原子多,证明A的金属性一定比B强 | |
| C. | 适量的Cl2通入FeI2溶液中可发生反应:3Cl2+6FeI2═2FeCl3+4FeI3 | |
| D. | A的金属性比B的金属性强,则A一定可以在水溶液置换出B来 |
15.近几年来,我国多次出现大范围雾霾天气,许多城市发布PM2.5重度污染警报.下列行为能缓解城市大气中PM2.5浓度的是( )
| A. | 燃放烟花爆竹 | B. | 为城市主干道洒水保洁 | ||
| C. | 大面积开发土建项目 |
12.将足量的铜屑加入到100mL浓度均为2mol.L-1的HNO3和H2SO4的混合溶液中,充分反应后,转移电子的物质的量为( )
| A. | 0.45mol | B. | 0.8mol | C. | 0.6mol | D. | 0.4mol |
 某温度时,在1L密闭容器中,A、B、C三种气态物质的物质的量随时间变化的曲线如图所示.由图中数据分析:
某温度时,在1L密闭容器中,A、B、C三种气态物质的物质的量随时间变化的曲线如图所示.由图中数据分析: