题目内容
下列排列顺序正确的是( )
①热稳定性:HF>H2O>NH3
②离子半径:Na+>Mg2+>F-
③电子数:H2O>OH->-OH
④结合质子能力:OH->C6H5O->HCO3-
⑤分散系中分散质粒子的直径:Fe(OH)3悬浊液>Fe(OH)3胶体>FeCl3溶液.
①热稳定性:HF>H2O>NH3
②离子半径:Na+>Mg2+>F-
③电子数:H2O>OH->-OH
④结合质子能力:OH->C6H5O->HCO3-
⑤分散系中分散质粒子的直径:Fe(OH)3悬浊液>Fe(OH)3胶体>FeCl3溶液.
| A、①③⑤ | B、①④⑤ |
| C、②④ | D、全部 |
考点:元素周期律的作用
专题:元素周期律与元素周期表专题
分析:①非金属性越强,对应氢化物的稳定性越强;
②具有相同核外电子排布的,原子序数越大,离子半径越小;
③H2O的电子数为10,OH-的电子数为10,-OH的电子数为9;
④酸性越强,对应离子结合质子的能力越弱;
⑤分散质微粒直径:悬浊液>胶体>溶液.
②具有相同核外电子排布的,原子序数越大,离子半径越小;
③H2O的电子数为10,OH-的电子数为10,-OH的电子数为9;
④酸性越强,对应离子结合质子的能力越弱;
⑤分散质微粒直径:悬浊液>胶体>溶液.
解答:
解:①非金属性越强,对应氢化物的稳定性越强,非金属性:F>O>N,则热稳定性:HF>H2O>NH3,故①正确;
②Na+、Mg2+和F-具有相同的核外电子排布,原子序数Mg>Na>F,所以离子半径F->Na+>Mg2+,故②错误;
③H2O的电子数为10,OH-的电子数为10,-OH的电子数为9,故电子数:H2O=OH->-OH,故③错误;
④酸性碳酸>苯酚,水为中性,酸性越强,离子的结构质子的能力越弱,故结合质子能力:OH->C6H5O->HCO3-,故④正确;
⑤分散质微粒直径:悬浊液>胶体>溶液,故Fe(OH)3悬浊液>Fe(OH)3胶体>FeCl3溶液,故⑤正确,
故排列顺序正确的是①④⑤,
故选B.
②Na+、Mg2+和F-具有相同的核外电子排布,原子序数Mg>Na>F,所以离子半径F->Na+>Mg2+,故②错误;
③H2O的电子数为10,OH-的电子数为10,-OH的电子数为9,故电子数:H2O=OH->-OH,故③错误;
④酸性碳酸>苯酚,水为中性,酸性越强,离子的结构质子的能力越弱,故结合质子能力:OH->C6H5O->HCO3-,故④正确;
⑤分散质微粒直径:悬浊液>胶体>溶液,故Fe(OH)3悬浊液>Fe(OH)3胶体>FeCl3溶液,故⑤正确,
故排列顺序正确的是①④⑤,
故选B.
点评:本题考查元素周期律的应用、电子数的计算、分散系等知识,综合性较强,难度中等.要注意基础知识的理解掌握.

练习册系列答案
相关题目
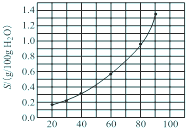 溴酸银(AgBrO3)的溶解度随温度变化曲线如图所示,下列说法错误的是( )
溴酸银(AgBrO3)的溶解度随温度变化曲线如图所示,下列说法错误的是( )| A、温度升高时溴酸银溶解速度加快 |
| B、溴酸银的溶解是放热过程 |
| C、60℃时,溴酸银的Ksp约等于6×10-4 |
| D、常温下溴酸银微溶于水 |
应用元素周期律分析下列推断,其中正确的是( )
| A、酸性强弱:HClO>H2SO4>H2CO3 |
| B、热稳定性:HF>HCl>HBr |
| C、已知硒(Se)与硫同主族,其最高价氧化物对应的水化物分子式为:H2SeO3 |
| D、原子半径大小:Na>P>N |
下列说法中正确的是( )
| A、在酸性环境中钢铁发生析氢腐蚀 |
| B、电解质溶液为氢氧化钠溶液,铝和镁形成原电池时,镁作负极 |
| C、铅蓄电池中铅做正极,PbO2做负极,两极浸在H2SO4溶液中 |
| D、镀层破损后,白铁(镀锌的铁)比马口铁(镀锡的铁)更易被腐蚀 |
将一定质量的锌粉与100mL 18.5mol?L-1的浓H2SO4混合,充分反应后锌完全溶解,生成了标准状况下的混合气体33.6L(设浓H2SO4的还原产物只有SO2,稀硫酸只生成H2),将反应后的溶液稀释成1L时,溶液pH=1,参加反应的锌为( )
| A、0.9 mol |
| B、1.2 mol |
| C、1.5 mol |
| D、1.8 mol |
宇宙飞船是用N2H4联氨与N2O4作为推力能源,其未配平的反应式为N2H4+N2O4→N2+H2O下列说法正确的是
( )
( )
| A、N2既是氧化产物又是还原产物 |
| B、氧化产物与还原产物物质的量之比为1:2 |
| C、联氨是氧化剂 |
| D、氧化剂与还原剂物质的量之比为2:1 |
 油价的持续“高烧”,引发人们对未来能源供需及价格的深切关注,并且促使人们寻求石油的替代品.
油价的持续“高烧”,引发人们对未来能源供需及价格的深切关注,并且促使人们寻求石油的替代品.