题目内容
某无色溶液能使紫色石蕊试液变红色,经实验测得该溶液中存在Ba2+和NO3-,则该溶液中还可能大量存在的离子组是( )
| A、NH4+、Mg2+、Cl-、K+ |
| B、Fe2+、Na+、Cl-、I- |
| C、SO42-、HCO3-、Cl-、K+ |
| D、AlO2-、Na+、Cl-、OH- |
考点:离子共存问题
专题:离子反应专题
分析:无色溶液中不存在Cu2+、Fe2+、Fe3+、MnO4-等有色离子;能使紫色石蕊试液变红色的溶液为酸性溶液;酸性溶液中硝酸根离子具有强氧化性;与钡离子反应的离子不能大量共存,
A.NH4+、Mg2+、Cl-、K+离子之间不发生反应,且都是无色离子、都不与氢离子、钡离子和硝酸根离子反应;
B.该溶液具有强氧化性,能够氧化亚铁离子、碘离子;
C.碳酸氢根离子能够与氢离子反应、硫酸根离子与钡离子反应生成硫酸钡沉淀;
D.偏铝酸根离子、氢氧根离子与氢离子反应.
A.NH4+、Mg2+、Cl-、K+离子之间不发生反应,且都是无色离子、都不与氢离子、钡离子和硝酸根离子反应;
B.该溶液具有强氧化性,能够氧化亚铁离子、碘离子;
C.碳酸氢根离子能够与氢离子反应、硫酸根离子与钡离子反应生成硫酸钡沉淀;
D.偏铝酸根离子、氢氧根离子与氢离子反应.
解答:
解:无色溶液中排除Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在;能使紫色石蕊试液变红色的溶液中存在大量氢离子;酸性溶液中NO3-离子具有强氧化性;与Ba2+离子反应的离子不能大量共存,
A.NH4+、Mg2+、Cl-、K+离子之间不反应,都不与酸溶液反应,也不与Ba2+和NO3-反应,且为无色溶液,在溶液中能够大量共存,故A正确;
B.酸性溶液中NO3-离子具有强氧化性,能够氧化Fe2+、I-离子,在溶液中不能大量共存,故B错误;
C.HCO3-与氢离子反应生成二氧化碳气体,SO42-与Ba2+反应生成硫酸钡沉淀,在溶液中不能大量共存,故C错误;
D.AlO2-、OH-都与氢离子反应,在溶液中不能大量共存,故D错误;
故选A.
A.NH4+、Mg2+、Cl-、K+离子之间不反应,都不与酸溶液反应,也不与Ba2+和NO3-反应,且为无色溶液,在溶液中能够大量共存,故A正确;
B.酸性溶液中NO3-离子具有强氧化性,能够氧化Fe2+、I-离子,在溶液中不能大量共存,故B错误;
C.HCO3-与氢离子反应生成二氧化碳气体,SO42-与Ba2+反应生成硫酸钡沉淀,在溶液中不能大量共存,故C错误;
D.AlO2-、OH-都与氢离子反应,在溶液中不能大量共存,故D错误;
故选A.
点评:本题考查离子共存的正误判断,题目难度中等,注意掌握离子反应发生条件,明确离子不能大量共存的一般情况,如:能发生复分解反应的离子之间; 能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的颜色,如无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在.

练习册系列答案
相关题目
下列有关化学用语中不能体现氮原子核外电子能量有差异的是( )
A、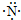 |
B、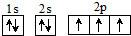 |
C、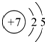 |
| D、1s22s22p3 |
下列说法正确的是( )
| A、蔗糖水解只生成葡萄糖 |
| B、含有碳碳双键的有机物均存在顺反异构现象 |
| C、向混有苯酚的苯中加入金属Na有无色气体生成 |
| D、用酸性高锰酸钾溶液检验CH2=CHCHO中是否含有醛基放电充电 |
NA为阿伏伽德罗常数的值,下列叙述正确的是( )
| A、1 L 1 mol?L-1的氯化铁溶液中铁离子的数目为NA |
| B、标准状况下,2.24L CH2Cl2含有的分子数为0.1NA |
| C、78g Na2O2固体与足量H2O反应转移的电子数为NA |
| D、t℃时,1L pH=6的纯水中OH-的数目为10-8NA |
甲烷的燃热为890kJ/mol,下列热化学方程式正确的是( )
| A、CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=+890kJ/mol |
| B、CH4+2O2═CO2+2H2O△H=-890kJ/mol |
| C、CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890kJ/mol |
| D、CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890kJ/mol |