题目内容
 反应A(g)+B(g)?c(g)+D(g)过程中的能量变化如图所示,回答下列问题.
反应A(g)+B(g)?c(g)+D(g)过程中的能量变化如图所示,回答下列问题.(1)图中a、b分别表示:a:
(2)该反应是
(3)当反应达到平衡时,升高温度,A的转化率
考点:反应热和焓变,化学平衡的影响因素
专题:化学反应中的能量变化,化学平衡专题
分析:(1)由图可知a为正反应的活化能;b为反应物与生成物能量差;
(2)根据反应物与生成物能量的相对大小分析;
(3)根据温度对平衡的影响分析.
(2)根据反应物与生成物能量的相对大小分析;
(3)根据温度对平衡的影响分析.
解答:
解:(1)由图可知a为反应物分子断键变成原子所吸收的能量,为正反应的活化能;b为反应物与生成物能量差,是反应的热效应即反应热;
故答案为:活化能;反应热;
(2)由图可知反应物具有的总能量大于生成物具有的总能量,所以该反应为放热反应;
故答案为:放热反应;
(3)已知该反应为放热反应,所以升高温度平衡逆移,则转化率减小,
故答案为:减小;该反应的正反应为放热反应,升高温度使平衡向逆反应方向移动.
故答案为:活化能;反应热;
(2)由图可知反应物具有的总能量大于生成物具有的总能量,所以该反应为放热反应;
故答案为:放热反应;
(3)已知该反应为放热反应,所以升高温度平衡逆移,则转化率减小,
故答案为:减小;该反应的正反应为放热反应,升高温度使平衡向逆反应方向移动.
点评:本题考查了反应中能量的变化,温度对平衡及转化率的影响,题目难度不大.

练习册系列答案
 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案
相关题目
下列各组离子在给定条件下一定能大量共存的是( )
| A、无色溶液中:K+、Na+、MnO4-、SO42- |
| B、含有大量NO3-的溶液中:NH4+、I-、SO42-、H+ |
| C、加入Al能放出H2的溶液中:Cl-、SO42-、NO3-、Mg2+ |
| D、在c(H+)=1.0×10-13mol?L-1的溶液中:Na+、SO42-、AlO-2、K+ |
下列解释实验现象的反应方程式正确的是( )
| A、向Cu(OH)2悬浊液中滴加Na2S溶液,蓝色沉淀变黑色Cu(OH)2(s)+S2-?CuS(s)+2OH- |
| B、在H2O2溶液中,滴加FeC13溶液产生气泡:2H2O2+2C1-=2H2O+O2↑+C12↑ |
| C、将相互接触的铜片和锌片置于稀硫酸中,铜片表面有气泡产生:Cu+2H+=Cu2++H2↑ |
| D、在CH3COONa溶液中,滴加酚酞变红:CH3COO-+H2O=CH3COOH+OH- |
下列不属于水解反应方程式的是( )
| A、NH4++H2O?NH3?H2O+H+ |
| B、MgCl2+2H2O?Mg(OH)2+2HCl |
| C、HCO3-+H2O?CO32-+H3O+ |
| D、ClO-+H2O?HClO+OH- |

 将0.1mol的镁铝混合物溶于100mL 1.5mol?L-1的H2SO4中,然后再滴加1mol?L-1的NaOH溶液.请回答:
将0.1mol的镁铝混合物溶于100mL 1.5mol?L-1的H2SO4中,然后再滴加1mol?L-1的NaOH溶液.请回答: 某实验小组采取如下步骤测定某苯酚样品的纯度.
某实验小组采取如下步骤测定某苯酚样品的纯度.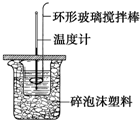 利用如图所示装置测定中和热的实验步骤如下:
利用如图所示装置测定中和热的实验步骤如下: