题目内容
15.下列分子中,所有原子不可能处在同一平面上的是( )| A. | CH4 | B. | CS2 | C. | H2O | D. | SO2 |
分析 在常见的有机化合物中甲烷是正四面体结构,CS2和H2O、SO2是平面型结构,是V型结构,其它有机物可在此基础上进行共线、共面判断.
解答 解:A、CH4是正四面体结构,因此所有原子不可能处于同一平面上,故A符合;
B、CS2具有平面型结构,类似于CO2的结构,所有原子在同一个平面,故B不符合;
C、H2O是V型平面结构,所有原子处于同一平面内,故C不符合;
D、SO2是平面结构,所有原子处于同一平面内,故D不符合;
故选:A.
点评 本题主要考查有机化合物的结构特点,做题时注意从CH4、CS2、H2O和SO2的结构特点判断分子的空间结构.

练习册系列答案
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案 口算心算速算应用题系列答案
口算心算速算应用题系列答案
相关题目
5.有X、Y两种元素,原子序数≤20,X的原子半径小于Y,且X、Y原子的最外层电子数相同(选项中m、n均为正整数).下列说法正确的是( )
| A. | 若HnXOm为强酸,则X的氢化物溶于水一定显酸性 | |
| B. | 若X(OH)n为强碱,则Y(OH)n也一定为强碱 | |
| C. | 若X元素形成的单质是X2,则Y元素形成的单质也一定是Y2 | |
| D. | 若Y的最高正化合价为+m,则X的最高正化合价一定为+m |
6.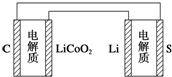 已知:锂离子电池的总反应为LixC+Li1-xCoO2$?_{充电}^{放电}$C+LiCoO2锂硫电池的总反应为2Li+S$?_{充电}^{放电}$Li2S有关上述两种电池说法正确的是( )
已知:锂离子电池的总反应为LixC+Li1-xCoO2$?_{充电}^{放电}$C+LiCoO2锂硫电池的总反应为2Li+S$?_{充电}^{放电}$Li2S有关上述两种电池说法正确的是( )
 已知:锂离子电池的总反应为LixC+Li1-xCoO2$?_{充电}^{放电}$C+LiCoO2锂硫电池的总反应为2Li+S$?_{充电}^{放电}$Li2S有关上述两种电池说法正确的是( )
已知:锂离子电池的总反应为LixC+Li1-xCoO2$?_{充电}^{放电}$C+LiCoO2锂硫电池的总反应为2Li+S$?_{充电}^{放电}$Li2S有关上述两种电池说法正确的是( )| A. | 锂离子电池放电时,Li+向负极迁移 | |
| B. | 锂硫电池充电时,锂电极发生氧化反应 | |
| C. | 理论上两种电池的比能量相同 | |
| D. | 下图表示用锂硫电池给锂离子电池充电 |
3.在d轨道中电子排布成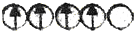 ,而不排布成
,而不排布成 ,其直接的根据是( )
,其直接的根据是( )
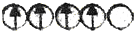 ,而不排布成
,而不排布成 ,其直接的根据是( )
,其直接的根据是( )| A. | 能量最低原理 | B. | 洪特规则 | C. | 原子轨道能级图 | D. | 泡利不相容原理 |
20.下列指定的比值为2:1的是( )
| A. | 0.2 mol/L 和0.1 mol/L的氨水中c(OH-)之比 | |
| B. | H2S溶液中c(H+)与c(S2-)之比 | |
| C. | Na2S溶液中c(Na+)与c(S2-)之比 | |
| D. | Na2O2晶体中阳离子与阴离子个数之比 |
7.设NA为阿伏伽德罗常数的值,下列叙述正确的是( )
| A. | 常温下1LpH=11的氨水中含有阳离子总数为0.001NA | |
| B. | 4g${\;}_{1}^{2}$H2中所含的质子数为4NA | |
| C. | 1mol甲醇中含有C-H键的数目为4NA | |
| D. | 常温常压下,22.4L的NO2和CO2混合气体含有2NA个氧原子 |
4.下列说法不正确的是( )
| A. | 分馏石油气和裂解气可用溴水进行鉴别 | |
| B. | 异丁烷的二氯取代物有3种(不考虑立体异构) | |
| C. | 主链含四个碳的烷烃中,碳原子个数是最多的是2,3-四甲基丁烷 | |
| D. | 乙醇和甘油都含羟基,葡萄糖和蔗糖都是糖类,但它们之间不是同系物 |
5.甲、乙、丙三种物质是某抗生素合成过程中的中间产物,下列说法正确的是( )
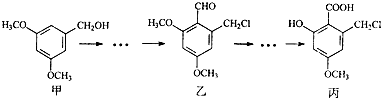

| A. | 甲、乙、丙三种有机化合物均可跟NaOH溶液反应 | |
| B. | 用FeCl3溶液区分甲、丙两种有机化合物 | |
| C. | 一定条件下丙可以与NaHCO3溶液、C2H5OH反应 | |
| D. | 乙、丙都能发生银镜反应 |