题目内容
5.某实验小组同学对电化学原理进行了一系列探究活动.
(1)如图1为某实验小组依据氧化还原反应:(用离子方程式表示)Fe+Cu2+═Fe2++Cu设计的原电池装置,反应前两电极质量相等,一段时间后,两电极质量相差12g,导线中转移0.2mol电子
(2)其它条件不变,若将CuCl2溶液换为NH4Cl溶液,石墨电极反应式为2H++2e-═H2↑;2H++2e-═H2↑;用吸管吸出铁片附近溶液少许于试管中,向其中滴加少量新制饱和氯水,写出发生反应的离子方程式2Fe2++Cl2═2Fe3++2Cl-,然后滴加几滴硫氰化钾溶液,溶液变红,继续滴加过量新制饱和氯水,颜色褪去,某同学的认为是“溶液中的+3价铁被氧化为更高的价态”,如果+3价铁被氯气氧化为FeO42-,写出该反应的离子方程式2Fe3++3Cl2+8H2O═2FeO42-+6Cl-+16H+.
(3)其它条件不变,若将盐桥换成弯铜导线与石墨相连成n型,如图2所示,一段时间后,在甲装置铜丝附近滴加酚酞试液,现象是溶液变红电极反应为O2+2H2O+4e-═4OH-乙装置中石墨(1)为阴极(填正、负、阴、阳),乙装置中与铜线相连石墨电极上的生成物常用湿润淀粉碘化钾试纸检验.
分析 (1)图1为原电池反应,Fe为负极,发生反应:Fe-2e-=Fe2-,石墨为正极,发生反应Cu2++2e-=Cu;
(2)若将CuCl2溶液换为NH4Cl溶液,溶液呈酸性,正极发生2H++2e-═H2↑,负极发生Fe-2e-=Fe2-,加入氯水发生2Fe2++Cl2═2Fe3++2Cl-;
(3)若将盐桥换成弯铜导线与石墨相连成n型,甲装置为铁的吸氧腐蚀,乙为电解池装置.
解答 解:(1)图1为原电池反应,Fe为负极,发生:Fe-2e-=Fe2-,石墨为正极,发生Cu2++2e-=Cu,总反应式为Fe+Cu2+═Fe2++Cu,一段时间后,两电极质量相差12g,
则Fe+Cu2+═Fe2++Cu 两极质量差△m 转移电子
56g 64g 56g+64g=120g 2mol
12g n
则:n=0.2mol,
故答案为:Fe+Cu2+═Fe2++Cu;0.2;
(2)若将CuCl2溶液换为NH4Cl溶液,溶液呈酸性,发生:NH4++H2O?NH3•H2O+H+,石墨电极正极发生2H++2e-═H2↑,负极发生反应:Fe-2e-=Fe2-,加入氯水发生反应:2Fe2++Cl2═2Fe3++2Cl-;如果+3价铁被氧化为FeO42-,发生反应为:2Fe3++3Cl2+8H2O═2FeO42-+6Cl-+16H+,
故答案为:2H++2e-═H2↑;2Fe2++Cl2═2Fe3++2Cl-;2Fe3++3Cl2+8H2O═2FeO42-+6Cl-+16H+;
(3)若将盐桥换成弯铜导线与石墨相连成n型,甲装置为铁的吸氧腐蚀,铁为负极,铜为正极,正极发生 O2+2H2O+4e-═4OH-,呈碱性,滴加酚酞,溶液变红,则乙装置铜为阳极,石墨为阴极,乙为电解池装置,阳极发生2Cl--2e-═Cl2↑,生成的氯气可用湿润淀粉碘化钾试纸检验,试纸变蓝,
故答案为:溶液变红; O2+2H2O+4e-═4OH-;阴;湿润淀粉碘化钾试纸.
点评 本题综合考查原电池和电解池知识,题目难度中等,侧重于电化学知识的综合运用的考查,注意明确电极反应方程式的书写方法,为解答该题的关键.

 活力课时同步练习册系列答案
活力课时同步练习册系列答案
已知:I.钒有多种价态,其中+5价最稳定.钒在溶液中主要以V02+和V03-的形式存在,存在平衡V02++H20?V03-+2H+.
Ⅱ.部分含钒物质在水中的溶解性如下表所示:
| 物质 | V205 | NH4V03 | (V02)2S04 |
| 溶解性 | 难溶 | 难溶 | 易溶 |
| Cu2+ | Fe2+ | Fe3+ | |
| 开始沉淀pH值 | 5.2 | 7.6 | 2.7 |
| 完全沉淀pH值 | 6.4 | 9.6 | 3.7 |
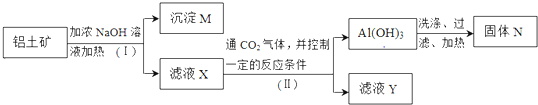
(1)碱浸步骤中最好选用a.
a.Na0H溶液b.氨水 c.纯碱溶液
(2)写出滤液1与足量二氧化碳反应的离子方程式AlO2-+CO2+2H2O=Al(OH)3+HCO3-;.
(3)磁选步骤得到的磁性产品为铁.
(4)溶液1到溶液2的过程中,调节pH值至8有两个目的,一是除去铜离子,二是使使VO2+转化为VO3-.
(5)滤渣3的主要成分为NH4VO3,工业上常用铝热反应法由V205冶炼金属钒,请写出反应的化学方程式3V205+10Al$\frac{\underline{\;高温\;}}{\;}$6V+5Al203.
| A. | v(H2)=0.03 mol/(L•min) | B. | v(N2)=0.02 mol/(L•min) | ||
| C. | v(NH3)=0.17 mol/(L•min) | D. | v(NH3)=0.01 mol/(L•min) |
①100mL水
②24mL 0.1mol•L-1 NaCl
③10mL 0.1mol•L-1 MgCl2
④30mL 0.1mol•L-1 AgNO3溶液中,各溶液中c(Ag+)由大到小的顺序为( )
| A. | ③①②④ | B. | ④③②① | C. | ①②③④ | D. | ④①②③ |
| A. | 羟基的电子式: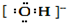 | B. | CH4分子的球棍模型: | ||
| C. | 乙烯的最简式:CH2 | D. | 氟离子的结构示意图: |
| 化学键 | H-H | H-Cl | H-Br | CI-CI | Br-Br |
| 键能( KJ•mol-1) | 436 | 431 | 299 | 247 | 193 |
| A. | HCl | B. | HBr | C. | H2 | D. | Br2 |
 .
. .
.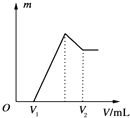 将0.1mol的镁、铝混合物溶于100mL、2mol•L-1的H2SO4溶液中,然后再滴加1mol•L-1的NaOH溶液.请回答:
将0.1mol的镁、铝混合物溶于100mL、2mol•L-1的H2SO4溶液中,然后再滴加1mol•L-1的NaOH溶液.请回答: