题目内容
9.按要求将化学方程式该为离子方程式2Na2O2+2H2O=4NaOH+O2↑2Na2O2+2H2O=4Na++4OH-+O2↑.分析 过氧化钠与水的反应中,过氧化钠、水和氧气都需要保留化学式,只有氢氧化钠可以拆开,据此将该化学方程式改成离子方程式.
解答 解:化学方程式2Na2O2+2H2O=4NaOH+O2↑中,Na2O2、H2O和O2↑都需要保留化学式,只有NaOH能够拆开,该反应的离子方程式为2Na2O2+2H2O=4Na++4OH-+O2↑,
故答案为:2Na2O2+2H2O=4Na++4OH-+O2↑.
点评 本题考查离子方程式的书写方法,题目难度不大,明确离子方程式的书写原则即可解答,试题侧重基础知识的考查,有利于提高学生的规范答题能力.

练习册系列答案
 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案
相关题目
4.常温下,浓度均为0.1mol/L的4种钠盐溶液pH如下:
下列说法不正确的是( )
| 溶质 | Na2CO3 | NaHCO3 | NaClO | NaHSO3 |
| pH | 11.6 | 9.7 | 10.3 | 5.28 |
| A. | 四种溶液中,Na2CO3溶液中水的电离程度最大 | |
| B. | 向氯水中加入少量NaHCO3(s),可以增大氯水中次氯酸的浓度 | |
| C. | NaHSO3溶液显酸性的原因是:NaHSO3=Na++H++SO32- | |
| D. | 常温下,相同物质的量浓度的H2SO3、H2CO3、HClO,pH最小的是H2SO3 |
1.在一定温度下的恒容密闭容器中,下列不是可逆反应A(g)+3B(g)?C(g)达到平衡标志的是( )
| A. | 3v正(A)=v逆(B) | |
| B. | 单位时间内生成a molA,同时生成3a molB | |
| C. | A、B、C的浓度不再变化 | |
| D. | 容器内的总压强不再变化 |
18.下列说法错误的是( )
| A. | 反应产物的总焓与反应物的总焓之差,称为反应焓变 | |
| B. | 反应产物的总焓小于反应物的总焓,该反应为吸收能量反应 | |
| C. | 同一反应在不同温度下进行,其焓变是不同的 | |
| D. | 同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的△H相同 |
19.下列陈述I、II均正确且有因果关系的是( )
| 选项 | 陈述I | 陈述II |
| A | Na2O2具有漂白性 | Na2O2可用于潜水呼吸用氧 |
| B | SiO2有导电性 | SiO2可用于制作光导纤维 |
| C | 浓H2SO4有脱水性 | 浓H2SO4可用于干燥Cl2、SO2 |
| D | CO有还原性 | CO可用来冶炼生铁 |
| A. | A | B. | B | C. | C | D. | D |
 锂-磷酸氧铜电池正极的活性物质是Cu4O(PO4)2,可通过下列反应制备:
锂-磷酸氧铜电池正极的活性物质是Cu4O(PO4)2,可通过下列反应制备: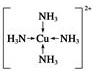 .
.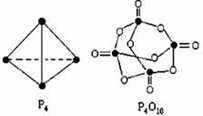 白磷与氧可发生如下反应:P4+5O2=P4O10.已知断裂下列化学键需要吸收的能量分别为:P-P akJ•mol-1、P-O bkJ•mol-1、P=O ckJ•mol-1、O=O dkJ•mol-1根据图示的分子结构和有关数据计算该反应的反应热(6a+5d-4c-12b)kJ•mol-1.
白磷与氧可发生如下反应:P4+5O2=P4O10.已知断裂下列化学键需要吸收的能量分别为:P-P akJ•mol-1、P-O bkJ•mol-1、P=O ckJ•mol-1、O=O dkJ•mol-1根据图示的分子结构和有关数据计算该反应的反应热(6a+5d-4c-12b)kJ•mol-1.