题目内容
某固体化合物A,按下图所示发生系列变化,已知E溶液中加入氨水后产生的白色沉淀很快变为灰绿色,最后变为红褐色.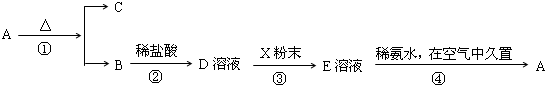
(1)请写出下列物质的化学式:A
(2)在①②③④各步反应中属于氧化还原反应的有
(3)请分别写出反应①的化学方程式和反应③的离子方程式:①
(1)依据推断可知A为Fe(OH)3,C为H2O,故答案为:Fe(OH)3;H2O;
(2)反应①是氢氧化铁分解生成氧化铁和水的反应,2Fe(OH)3
| ||
反应②是盐酸和氧化铁发生的复分解反应,Fe2O3+6HCl=2FeCl3+3H2O,不是氧化还原反应;
反应③是氯化铁和铁发生的氧化还原反应,Fe+2FeCl3=3FeCl2,氧化还原反应;
反应④是氢氧化亚铁和氧气水 发生反应生成氢氧化铁的也还原反应,反应化学方程式为4Fe(OH)2+O2+2H2O=4Fe(OH)3,是氧化还原反应;
故答案为:③④;
(3)反应①是氢氧化铁受热分解的反应,化学方程式为2Fe(OH)3
| ||
故答案为:2Fe(OH)3
| ||

 计算高手系列答案
计算高手系列答案(16分)某班学生在老师指导下探究氮的化合物的某些性质。
(1)同学甲在实验室利用下列装置(后面有图)制取氨气和氧气的混合气体,并完成氨的催化氧化。
A中加入浓氨水,D中加入碱石灰,E内放置催化剂(铂石棉),请回答:
①仪器B的名称:__________。B内只需加入一种固体试剂,该试剂的名称为_________,B中能产生氨气和氧气混合气体的原因(结合化学方程式回答)_ __。
②按气流方向连接各仪器 (填接口字母)
(2)同学乙拟用甲同学得到的混合气体X(NO及过量的NH3),验证NO能被氨气还原并测算其转化率(忽略装置内空气的影响)。装置如下:
①装置C的作用可能是 ____________。
②若进入装置A的NO共268.8mL(已折算为标准状况,下同),氨气过量,最后收集到标准状况下190.4 mL N2,则NO的转化率为 。
(3)N2O3是一种新型硝化剂。一定温度下,在恒容密闭容器中N2O3可发生下列反应:2N2O3+O24NO2(g);△H>0,下表为反应在某温度下的部分实验数据:
| t/s | 0 | 500 | 1000 |
| c(N2O3)/mol·L-1 | 5.00 | 3.52 | 2.48 |
计算在t=500s时,NO2的反应速率为 。
某班学生在老师指导下探究氮的化合物的某些性质。
(1)同学甲在实验室利用下列装置制取氨气和氧气的混合气体,并完成氨的催化氧化。
A中加入浓氨水,D中加入碱石灰,E内放置催化剂(铂石棉),请回答:
①仪器B的名称:_____________。B内只需加入一种固体试剂,该试剂的名称为__________,B中能产生氨气和氧气混合气体的原因(结合化学方程式回答)_ __。
②按气流方向连接各仪器 (填接口字母)
(2)同学乙拟用甲同学得到的混合气体X(NO及过量的NH3),验证NO能被氨气还原并测算其转化率(忽略装置内空气的影响w.w.^w.k.&s.5*u.c.#om)。装置如下:
①装置C的作用可能是 ____________
②若进入装置A的NO共268.8mL(已折算为标准状况,下同),氨气过量,最后收集到标准状况下190.4 mL N2,则NO的转化率为
(3)N2O3是一种新型硝化剂。一定温度下,在恒容密闭容器中N2O3可发生下列反应:2N2O3+O2 4NO2(g);△H>0,下表为反应在某温度下的部分实验数据
4NO2(g);△H>0,下表为反应在某温度下的部分实验数据
| t/sw.w.^w.k.&s.5*u.c.#om | 0w.w.^w.k.&s.5*u.c.#om | 500 | 1000 |
| c(N2O3)/mol·L-1 | 5.00 | 3.52w.w.^w.k.&s.5*u.c.#om | 2.48 |
(16分)某班学生在老师指导下探究氮的化合物的某些性质。
(1)同学甲在实验室利用下列装置(后面有图)制取氨气和氧气的混合气体,并完成氨的催化氧化。
A中加入浓氨水,D中加入碱石灰,E内放置催化剂(铂石棉),请回答:
①仪器B的名称:__________。B内只需加 入一种固体试剂,该试剂的名称为_________,B中能产生氨气和氧气混合气体的原
入一种固体试剂,该试剂的名称为_________,B中能产生氨气和氧气混合气体的原 因(结合化学方程式回答)_ __。
因(结合化学方程式回答)_ __。
②按气流方向连接各仪器 (填接口字母)
(2)同学乙拟用甲同学得到的混合气体X(NO及过量的NH3),验证NO能被氨气还原并测算其转化率(忽略装置内空气的影响)。装置如下:
①装置C的作用可能是 ____________。
②若进入装置A的NO共268.8mL(已折算为标准状况,下同),氨气过量,最后收集到标准状况下190.4 mL N2,则NO的转化率为 。
(3)N2O3是一种新型硝化剂。一定温度下,在恒容密闭容器中N2O3可发生下列反应:2N2O3+O2 4NO2(g);△H>0,下表为反应在某温度下的部分实验数据:
4NO2(g);△H>0,下表为反应在某温度下的部分实验数据:
| t/s | 0 | 500 | 1000 |
| c(N2O3)/mol·L-1 | 5.00 | 3.52 | 2.48 |
计算在t=500s时,NO2的反应速率为 。
(16分)某班学生在老师指导下探究氮的化合物的某些性质。
(1)同学甲在实验室利用下列装置(后面有图)制取氨气和氧气的混合气体,并完成氨的催化氧化。
A中加入浓氨水,D中加入碱石灰,E内放置催化剂(铂石棉),请回答:
①仪器B的名称:__________。B内只需加入一种固体试剂,该试剂的名称为_________,B中能产生氨气和氧气混合气体的原因(结合化学方程式回答)_ __。
②按气流方向连接各仪器 (填接口字母)

(2)同学乙拟用甲同学得到的混合气体X(NO及过量的NH3),验证NO能被氨气还原并测算其转化率(忽略装置内空气的影响)。装置如下:

①装置C的作用可能是 ____________。
②若进入装置A的NO共268.8mL(已折算为标准状况,下同),氨气过量,最后收集到标准状况下190.4 mL N2,则NO的转化率为 。
(3)N2O3是一种新型硝化剂。一定温度下,在恒容密闭容器中N2O3可发生下列反应:2N2O3+O2 4NO2(g);△H>0,下表为反应在某温度下的部分实验数据:
4NO2(g);△H>0,下表为反应在某温度下的部分实验数据:
|
t/s |
0 |
500 |
1000 |
|
c(N2O3)/mol·L-1 |
5.00 |
3.52 |
2.48 |
计算在t=500s时,NO2的反应速率为 。