题目内容
6.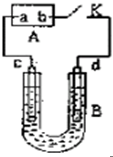 如图,A为直流电源,B为电解槽,c、d为石墨电极,B中存放有100mL NaCl和CuCl2的混合溶液,其中Cu2+的物质的量浓度为0.1mol/L,闭合K,d极收集到标准状况下448mL的一种气体甲,该气体能使湿润的碘化钾淀粉试纸变蓝.气体体积均在标准状况下测定,假设溶液的体积变化忽略不计,不考虑电解产生的气体溶解和吸收.请回答下列问题.
如图,A为直流电源,B为电解槽,c、d为石墨电极,B中存放有100mL NaCl和CuCl2的混合溶液,其中Cu2+的物质的量浓度为0.1mol/L,闭合K,d极收集到标准状况下448mL的一种气体甲,该气体能使湿润的碘化钾淀粉试纸变蓝.气体体积均在标准状况下测定,假设溶液的体积变化忽略不计,不考虑电解产生的气体溶解和吸收.请回答下列问题.(1)A电源的a极是负极
(2)计算c极理论上收集到的气体的体积是0.224L(标准状况下).
(3)假设100mL溶液中,c(Cu2+)=a mol/L,c(Na+)=b mol/L,Cu2+完全放电后,理论上d极产生甲气体的体积V范围是2.24aL≤V≤(2.24a+1.12b)L(用带a、b的代数式表示).
分析 d极收集到标准状况下448mL的一种气体甲,该气体能使湿润的碘化钾淀粉试纸变蓝,则d极收集的气体为氯气,d极的电极方程式为:2Cl--2e-=Cl2↑,所以d为阳极,则b为正极,a为负极,c为阴极,阴极上先铜离子得电子,后氢离子得电子,则发生的电极反应为:Cu2++2e-=Cu,2H++2e-=H2↑,结合电子守恒进行计算分析.
解答 解:d极收集到标准状况下448mL的一种气体甲,该气体能使湿润的碘化钾淀粉试纸变蓝,则d极收集的气体为氯气,d极的电极方程式为:2Cl--2e-=Cl2↑,所以d为阳极,则b为正极,a为负极,c为阴极,阴极上先铜离子得电子,后氢离子得电子,则发生的电极反应为:Cu2++2e-=Cu,2H++2e-=H2↑,
(1)A电源的a极是负极;故答案为:负极;
(2)d极的电极方程式为:2Cl--2e-=Cl2↑,氯气为0.448L,则其物质的量为0.02mol,所以转移电子为0.04mol,n(Cu2+)=0.1mol/L×0.1L=0.01mol,所以铜离子得到的电子为0.02mol,氢离子得到的电子为0.04mol-0.02mol=0.02mol,由2H++2e-=H2↑可知,生成的氢气为0.01mol,其体积为0.01mol×22.4L/mol=0.224L;
(3)若只发生CuCl2$\frac{\underline{\;通电\;}}{\;}$Cu+Cl2↑,则n(Cu)=0.1amol,V(Cl2)=0.1amol×22.4L/mol=2.24aL,
若发生CuCl2$\frac{\underline{\;通电\;}}{\;}$Cu+Cl2↑,后又发生2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑,第一个反应生成氯气为2.24aL,第二个反应生成氯气为0.1bmol×$\frac{1}{2}$×22.4L/mol=21.12bL,则一共生成2.24a+1.12bL,所以理论上d极产生甲气体的体积V范围是2.24aL≤V≤(2.24a+1.12b)L;
故答案为:2.24aL≤V≤(2.24a+1.12b)L.
点评 本题考查学生有关电解池的工作原理知识,注意把握阴阳两极上离子的放电顺序,明确电极反应式中电子与各物质之间的关系是解题的关键,题目难度中等.

 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案2CH3OH+3O2+4OH-$?_{充电}^{放电}$ 2CO32-+6H2O则下列说法错误的( )
| A. | 放电时CH3OH参与反应的电极为正极 | |
| B. | 充电时电解质溶液的pH逐渐增大 | |
| C. | 放电时负极的电极反应为:2CH3OH-12e-+16OH-═2CO32-+12H2O | |
| D. | 充电时每生成1 mol CH3OH转移6 mol电子 |
| A. | 氯水 | B. | 乙烯 | C. | 乙醇 | D. | 碘化钾溶液 |
| A. | 甲苯苯环上的一个氢原子被含3个碳原子的烷基取代所得产物有6种 | |
| B. | 与 互为同分异构体的芳香族化合物有6种 互为同分异构体的芳香族化合物有6种 | |
| C. | 2-甲基丁烷的一氯取代物共有4种 | |
| D. | 菲的结构简式为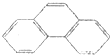 ,它的一硝基取代物有5种 ,它的一硝基取代物有5种 |
| A. | Cu+2Fe3+═Cu2++2Fe2+ | |
| B. | 1OCI-+2MnO4一+16H+═2Mn2++5Cl2↑+8H2O | |
| C. | 2Cu+C12$\frac{\underline{\;点燃\;}}{\;}$2CuC12 | |
| D. | 5Pb2++2MnO4一+2H2O═5PbO2+2Mn2++4H+ |
| A. | ③④ | B. | ②③④ | C. | ①③④ | D. | ①②③④ |
| A. | 稀硝酸 | B. | 浓硝酸 | C. | 浓硫酸 | D. | 浓盐酸 |
| A. | 液氨致冷 | B. | 电解制铝 | C. | 钙基固硫 | D. | 高炉炼铁 |
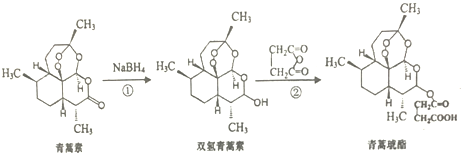
| A. | 青嵩素分子式为C15H23O5 | B. | 青嵩素不能与NaOH溶液反应 | ||
| C. | 反应②原子利用率为100% | D. | 青嵩琥不能与碳酸氢钠溶液反应 |