题目内容
下列物质中,既有离子键,又有共价键的是( )
| A、CaCl2 |
| B、Na2O |
| C、H2O |
| D、NaOH |
考点:离子化合物的结构特征与性质,共价键的形成及共价键的主要类型
专题:化学键与晶体结构
分析:一般来说,活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,碱金属族元素、第IIA族元素和第VIA族、第VIIA族元素之间易形成离子键,铵盐中含有离子键,据此分析解答.
解答:
解:A.氯化钙中氯离子和钙离子之间只存在离子键,故A错误;
B.氧化钠中钠离子和银离子之间只存在离子键,故B错误;
C.水分子中O原子和H原子之间只存在共价键,故C错误;
D.NaOH中钠离子和氢氧根离子之间、O原子和H原子之间只存在共价键,故D正确;
故选D.
B.氧化钠中钠离子和银离子之间只存在离子键,故B错误;
C.水分子中O原子和H原子之间只存在共价键,故C错误;
D.NaOH中钠离子和氢氧根离子之间、O原子和H原子之间只存在共价键,故D正确;
故选D.
点评:本题考查离子键和共价键的判断,侧重考查基本概念,明确物质的构成微粒及微粒间作用力即可解答,注意不能根据是否含有金属元素判断离子键,为易错点.

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
相关题目
氧化镁、碳酸氢钠、氢氧化铝、碳酸钙均可用于治疗胃酸(主要成分是盐酸)过多.它们分别与盐酸反应,依次对应的离子方程式正确的是( )
| A、MgO+2H+=Mg2++H2O |
| B、CO32-+2H+=CO2↑+H2O |
| C、OH-+H+=H2O |
| D、CaCO3+H+=Ca2++CO2↑+H2O |
下列有机物是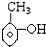 的同系物的是( )
的同系物的是( )
 的同系物的是( )
的同系物的是( )A、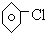 |
B、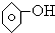 |
C、 |
D、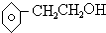 |
丙烷的六氯代物的同分异构体数目有( )
| A、2种 | B、3种 | C、4种 | D、5种 |
原子序数大于4的主族元素X、Y的离子Xm+、Yn-,它们的核外电子排布相同,则下列关于X、Y元素的说法正确的是( )
| A、Xm+的半径大于Yn-的半径 |
| B、X和Y处在同一周期 |
| C、Y和X的族序数之差是8-m-n |
| D、X和Y的核电荷数之差是m-n |
下列各组离子中,能在液体中大量共存的是( )
| A、Na+、H+、NO3-、OH- |
| B、Ca2+、NO3-、HCO3-、OH- |
| C、K+、H+、Cl-、SO42- |
| D、Fe3+、Cl-、H+、CO32- |