题目内容
(1)一定温度下,在一个固定容积的密闭容器中,可逆反应A(g)+2B(g)?4C(g)△H>0 达到平衡时,c(A)=2mol/L,c(B)=7mol/L,c(C)=4mol/L.试确定B的起始浓度c(B)的取值范围是 ;若改变条件重新达到平衡后体系中C的体积分数增大,下列措施可行的是 .
①增加C的物质的量 ②加 压 ③升 温 ④使用催化剂
(2)25℃,柠檬水的pH是3,其中c(OH-)═ ;KW= .
(3)某温度(t℃)时,水的离子积为KW=1×10-13,则该温度(选填“大于”“小于”或“等于”) 25℃.
(4)下列溶液中,c(H+)由小到大的排列顺序是
①0.1mol/L HCl 溶液 ②0.1mol/L H2SO4 溶液
③0.1mol/L NaOH溶液 ④0.1mol/L CH3COOH溶液.
①增加C的物质的量 ②加 压 ③升 温 ④使用催化剂
(2)25℃,柠檬水的pH是3,其中c(OH-)═
(3)某温度(t℃)时,水的离子积为KW=1×10-13,则该温度(选填“大于”“小于”或“等于”)
(4)下列溶液中,c(H+)由小到大的排列顺序是
①0.1mol/L HCl 溶液 ②0.1mol/L H2SO4 溶液
③0.1mol/L NaOH溶液 ④0.1mol/L CH3COOH溶液.
考点:化学平衡的影响因素,离子积常数
专题:化学平衡专题,电离平衡与溶液的pH专题
分析:(1)若A完全转化为C,B取最小值,若C完全转化为反应物,B取最大值;改变条件重新达到平衡后体系中C的体积分数增大,可使平衡正向移动或增加C;
(2)依据常温下水溶液中存在离子键常数为10-14,根据Kw=c(OH-)×c(H+)=1×10-14以及pH=-lg[c(H+)]计算;
(3)水的电离是吸热反应,升高温度促进水电离,则溶液的离子积常数增大;
(4)依据溶液中离子浓度大小和离子积常数计算分析溶液中氢离子浓度;
(2)依据常温下水溶液中存在离子键常数为10-14,根据Kw=c(OH-)×c(H+)=1×10-14以及pH=-lg[c(H+)]计算;
(3)水的电离是吸热反应,升高温度促进水电离,则溶液的离子积常数增大;
(4)依据溶液中离子浓度大小和离子积常数计算分析溶液中氢离子浓度;
解答:
解:(1)可逆反应A(g)+2B(g)?4C(g)△H>0达到平衡时,c(A)=2mol/L,c(B)=7mol/L,c(c)=4mol/L,若A完全转化为C,消耗B为04mol/L,则B最小值为3mol/L,若C完全转化为反应物,生成2molB,则B的最大值为9mol/L,因反应为可逆反应,均不能完全转化,则B的浓度范围为3mol/L<c(B)<9mol/L;
若改变条件重新达到平衡后体系中C的质量分数增大,应使平衡向正反应方向移动,
①增加C的物质的量,等效为增大压强,平衡向逆反应方向移动,C的质量分数降低,故①错误;
②加压,平衡向逆反应方向移动,C的质量分数降低,故②错误;
③升温,平衡向正反应方向移动,C的质量分数增大,故③正确;
④使用催化剂,平衡不移动,C的质量分数不变,故④错误;
故选③,
故答案为:3mol/L<c(B)<9mol/L;③;
(2)柠檬水溶液的pH=3,则c(H+)=1×10-3mol/L,因Kw=c(OH-)×c(H+)=1×10-14,则c(OH-)=1×10-11mol?L-1;
故答案为:1×10-11mol/L,1×10-14 ;
(3)水的电离是吸热反应,升高温度促进水电离,则水的离子积常数增大,某温度(T℃)时,水的离子积常数Kw=1×10-13>10-14,则该温度大于25℃,
故答案为:大于;
(4)①0.1mol/L HCl 溶液,c(H+)=0.1mol/L;
②0.1mol/L H2SO4 溶液中c(H+)=0.2mol/L;
③0.1mol/L NaOH溶液中c(H+)=
=10-13mol/L;
④0.1mol/L CH3COOH溶液,存在电离平衡,溶液中氢离子浓度小于0.1mol/L;
溶液中c(H+)由小到大的排列顺序③④①②;
故答案为:③④①②;
若改变条件重新达到平衡后体系中C的质量分数增大,应使平衡向正反应方向移动,
①增加C的物质的量,等效为增大压强,平衡向逆反应方向移动,C的质量分数降低,故①错误;
②加压,平衡向逆反应方向移动,C的质量分数降低,故②错误;
③升温,平衡向正反应方向移动,C的质量分数增大,故③正确;
④使用催化剂,平衡不移动,C的质量分数不变,故④错误;
故选③,
故答案为:3mol/L<c(B)<9mol/L;③;
(2)柠檬水溶液的pH=3,则c(H+)=1×10-3mol/L,因Kw=c(OH-)×c(H+)=1×10-14,则c(OH-)=1×10-11mol?L-1;
故答案为:1×10-11mol/L,1×10-14 ;
(3)水的电离是吸热反应,升高温度促进水电离,则水的离子积常数增大,某温度(T℃)时,水的离子积常数Kw=1×10-13>10-14,则该温度大于25℃,
故答案为:大于;
(4)①0.1mol/L HCl 溶液,c(H+)=0.1mol/L;
②0.1mol/L H2SO4 溶液中c(H+)=0.2mol/L;
③0.1mol/L NaOH溶液中c(H+)=
| 10-14 |
| 0.1 |
④0.1mol/L CH3COOH溶液,存在电离平衡,溶液中氢离子浓度小于0.1mol/L;
溶液中c(H+)由小到大的排列顺序③④①②;
故答案为:③④①②;
点评:本题考查了化学平衡影响因素分析判断,水溶液中离子积常数的计算应用,注意弱电解质存在电离平衡,题目难度中等.

练习册系列答案
 智慧小复习系列答案
智慧小复习系列答案
相关题目
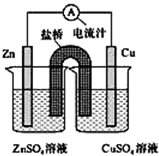 如图为一原电池的装置示意图,下列说法不正确的是( )
如图为一原电池的装置示意图,下列说法不正确的是( )| A、原电池工作时的总反应为:Zn+Cu2+=Zn2++Cu |
| B、原电池工作时,电流由铜极流经电流计流向锌极 |
| C、原电池工作时,盐桥中K+移向CuSO4溶液 |
| D、如果将Cu电极与Zn电极互换,电流计指针反向偏转 |
下列各组离子,能在水溶液中大量共存的是( )
| A、OH-、K+、Fe3+、NO3- |
| B、HCO3-、OH-、Cl-、K+ |
| C、Mg2+、NO3-、H+、Al3+ |
| D、SO42-、Ag+、NH4+、Cl- |
下列变化必须加还原剂才能发生的是( )
| A、Na2CO3→NaHCO3 | ||
| B、H2O2→H2O | ||
| C、Cu→CuO | ||
D、MnO
|