题目内容
14.X、Y、Z、W、Q都是短周期主族元素,其中X是短周期原子半径最大的元素,X与Y处于同一周期,Y与Z同主族且能形成两种常见的化合物,W能形成两种简单的离子,Q原子的电子总数等于其电子层数的3倍.下列说法正确的是( )| A. | 元素Q是短周期非金属性最强的元素 | |
| B. | Y、Z形成的化合物中只有一种属于酸性氧化物 | |
| C. | Y、Z、Q分别与W形成的化合物中,Z形成的化合物的沸点最高 | |
| D. | X分别与Y、Z、W形成的化合物中可能既含离子键又含共价键 |
分析 X、Y、Z、W、Q都是短周期主族元素,其中X是短周期原子半径最大的元素,则X为Na;X与Y处于同一周期,Y与Z同主族且能形成两种常见的化合物,则Y为S元素、Z为O元素;W能形成两种简单的离子,则W为H元素;Q原子的电子总数等于其电子层数的3倍,原子只能有2个电子层,核外电子数为6,故Q为C元素,据此解答.
解答 解:X、Y、Z、W、Q都是短周期主族元素,其中X是短周期原子半径最大的元素,则X为Na;X与Y处于同一周期,Y与Z同主族且能形成两种常见的化合物,则Y为S元素、Z为O元素;W能形成两种简单的离子,则W为H元素;Q原子的电子总数等于其电子层数的3倍,原子只能有2个电子层,核外电子数为6,故Q为C元素.
A.元素Q为碳元素,不是短周期非金属性最强的元素,短周期中非金属最强的元素为F元素,故A错误;
B.Y、Z形成的化合物为二氧化硫、三氧化硫,均属于酸性氧化物,故B错误;
C.Y、Z、Q分别与W形成的化合物为氢化物,分别为硫氢化、水、均为,由于水分子之间存在氢键,沸点最高,故C正确;
D.Na与氧元素形成的过氧化钠中既含离子键又含共价键,故D正确,
故选:CD.
点评 本题考查结构性质位置关系应用,推断元素是解题关键,注意能形成两种简单的离子的元素,难度中等.

练习册系列答案
相关题目
4.某实验小组用工业上废渣(主要成分Cu2S和Fe2O3)制取纯铜和绿矾(FeSO4•7H2O)产品,设计流程如图:
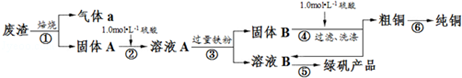
(1)在实验室中,欲用98%的浓硫酸(密度为1.84g•mL-1)配制500mL1.0mol•L-1的硫酸,需要的仪器除量筒、烧杯、玻璃棒外,还有胶头滴管、500mL容量瓶.
(2)该小组同学设计如图装置模拟废渣在过量氧气中焙烧,并验证废渣中含硫元素.

①装置A中反应的化学方程式为2Na2O2+2H2O=4NaOH+O2↑;为控制反应不过于激烈并产生平稳气流,采取的操作及现象是打开分液漏斗上口活塞,控制分液漏斗旋塞,使水匀速逐滴滴下;B处应连接盛有碱石灰的干燥管(或U形管)或浓硫酸的洗气瓶(填写试剂及仪器名称).
②E装置中加入品红溶液的目的是检验气体a中的SO2;当F装置中出现白色沉淀时,反应离子方程式为2SO2+O2+2H2O+2Ba2+=2BaSO4↓+4H+.
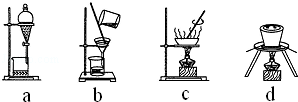
(3)下列操作中,不属于步骤⑤中进行的操作的是ad(填下列各项中序号).
(4)为测定产品中绿矾的质量分数,称取30.000g样品溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.1000mol•L-1酸性KMnO4溶液进行滴定,反应为:10FeSO4+8H2SO4+2KMnO4═2MnSO4+5Fe2(SO4)3+K2SO4+8H2O.实验所得数据如下表所示:
①第1组实验数据出现异常,造成这种异常的原因可能是ad(填代号).
a.酸式滴定管用蒸馏水洗净后未用标准液润洗 b.锥形瓶洗净后未干燥
c.滴定终点时俯视读数 d.滴定终点时仰视读数
②根据表中数据,计算所得产品中绿矾的质量分数为92.7%.

(1)在实验室中,欲用98%的浓硫酸(密度为1.84g•mL-1)配制500mL1.0mol•L-1的硫酸,需要的仪器除量筒、烧杯、玻璃棒外,还有胶头滴管、500mL容量瓶.
(2)该小组同学设计如图装置模拟废渣在过量氧气中焙烧,并验证废渣中含硫元素.

①装置A中反应的化学方程式为2Na2O2+2H2O=4NaOH+O2↑;为控制反应不过于激烈并产生平稳气流,采取的操作及现象是打开分液漏斗上口活塞,控制分液漏斗旋塞,使水匀速逐滴滴下;B处应连接盛有碱石灰的干燥管(或U形管)或浓硫酸的洗气瓶(填写试剂及仪器名称).
②E装置中加入品红溶液的目的是检验气体a中的SO2;当F装置中出现白色沉淀时,反应离子方程式为2SO2+O2+2H2O+2Ba2+=2BaSO4↓+4H+.
(3)下列操作中,不属于步骤⑤中进行的操作的是ad(填下列各项中序号).

(4)为测定产品中绿矾的质量分数,称取30.000g样品溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.1000mol•L-1酸性KMnO4溶液进行滴定,反应为:10FeSO4+8H2SO4+2KMnO4═2MnSO4+5Fe2(SO4)3+K2SO4+8H2O.实验所得数据如下表所示:
| 滴定次数 | 1 | 2 | 3 | 4 |
| KMnO4溶液体积/mL | 20.90 | 20.02 | 19.98 | 20.00 |
a.酸式滴定管用蒸馏水洗净后未用标准液润洗 b.锥形瓶洗净后未干燥
c.滴定终点时俯视读数 d.滴定终点时仰视读数
②根据表中数据,计算所得产品中绿矾的质量分数为92.7%.
5.工业上常回收冶炼锌废渣中的锌(含有ZnO、FeO、Fe2O3、CuO、Al2O3等杂质,并用来生产ZnSO4•6H2O晶体,其工艺流程如下,有关氢氧化物沉淀时的 pH 如下表.
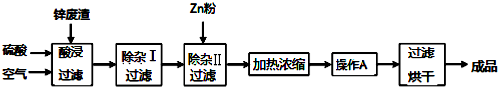
(1)上述工艺流程中多处涉及“过滤”,实验室中过滤操作需要使用的玻璃仪器有烧杯、玻璃棒、漏斗.
(2)在“除杂Ⅰ”步骤中,需再加入适量H2O2溶液的目的是将Fe2+完全氧化为Fe3+.为使 Fe(OH)3、Al(OH)3沉淀完全,而Zn(OH)2不沉淀,应控制溶液的pH范围为5.2~5.4.为控制上述pH范围可选择加入的试剂或药品是AD.
A.ZnO B.氨水 C.固体NaOH D.ZnCO3
(3)常温下,已知 Ksp[Zn(OH)2]=5×10-17,某 ZnSO4溶液里c(Zn2+)=0.5mol/L,如果要生成Zn(OH)2沉淀,则应调整溶液 pH 大于6.
(4)当向含相同浓度Cu2+、Fe3+、Fe2+的溶液中滴加某浓度的NaOH溶液时,Fe3+(填离子符号)先沉淀,Ksp[Fe(OH)2]>Ksp[Cu(OH)2](填“>”、“=”或“<”)

| 氢氧化物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Zn(OH)2 | Cu(OH)2 |
| 开始沉淀的 pH | 3.3 | 1.5 | 6.5 | 5.4 | 4.2 |
| 沉淀完全的 pH | 5.2 | 3.7 | 9.7 | 8.0 | 6.7 |
(2)在“除杂Ⅰ”步骤中,需再加入适量H2O2溶液的目的是将Fe2+完全氧化为Fe3+.为使 Fe(OH)3、Al(OH)3沉淀完全,而Zn(OH)2不沉淀,应控制溶液的pH范围为5.2~5.4.为控制上述pH范围可选择加入的试剂或药品是AD.
A.ZnO B.氨水 C.固体NaOH D.ZnCO3
(3)常温下,已知 Ksp[Zn(OH)2]=5×10-17,某 ZnSO4溶液里c(Zn2+)=0.5mol/L,如果要生成Zn(OH)2沉淀,则应调整溶液 pH 大于6.
(4)当向含相同浓度Cu2+、Fe3+、Fe2+的溶液中滴加某浓度的NaOH溶液时,Fe3+(填离子符号)先沉淀,Ksp[Fe(OH)2]>Ksp[Cu(OH)2](填“>”、“=”或“<”)
2.下列事实不用原电池原理解释的是( )
| A. | 轮船水线以下的船壳上装一定数量的锌块 | |
| B. | 红热的铁丝与冷水接触,表面形成蓝黑色保护层 | |
| C. | 纯锌与稀硫酸反应时,滴入少量CuSO4溶液后反应速率加快 | |
| D. | 烧过菜的铁锅加入清水放置,出现红棕色的锈斑 |
9.能测定Na2CO3和NaHCO3混合物中Na2CO3质量分数的实验方案是( )
| A. | 取a克混合物充分加热至质量不变,减重b克 | |
| B. | 取a克混合物与足量稀硝酸充分反应,加热、蒸干、灼烧至熔化,冷却得b克固体 | |
| C. | 取a克混合物与足量稀硫酸充分反应,逸出气体用碱石灰完全吸收,增重b克 | |
| D. | 取a克混合物与足量Ba(OH)2溶液充分反应,过滤、洗涤、烘干,得b克固体 |
19.卤族元素的单质和化合物很多,我们可以利用所学物质结构与性质的相关知识去认识和理解它们.
(1)卤族元素位于元素周期表的P区;溴的价电子排布式为4s24p5.
(2)在一定浓度的溶液中,氢氟酸是以二分子缔合(HF)2形式存在的.使氢氟酸分子缔合的作用力是氢键.
(3)请根据下表提供的第一电离能数据判断,最有可能生成较稳定的单核阳离子的卤素原子是碘(写出名称).
(4)已知碘酸(HIO3)和高碘酸(H5IO6)的结构分别如图1的Ⅰ、Ⅱ所示: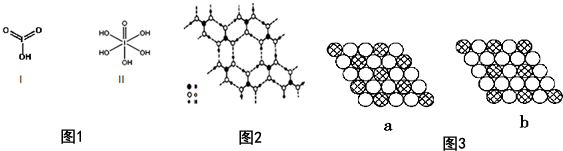
请比较二者酸性强弱:HIO3> H5IO6(填“>”、“<”或“=”).
(5)硼酸(H3BO3)是一种片层状结构的白色晶体,层内的H3B03分子间通过氢键相连(如图2).则1molH3BO3的晶体中有3 mol氢键.
硼酸溶于水生成弱电解质一水合硼酸B(OH)3•H2 O,它电离生成少量[B(OH)4]一和H+,则[B(OH)4]一含有的化学键类型为共价键、配位键.
(6)如图所示的二维平面晶体示意图3中表示化学式为AX3的是b.
(1)卤族元素位于元素周期表的P区;溴的价电子排布式为4s24p5.
(2)在一定浓度的溶液中,氢氟酸是以二分子缔合(HF)2形式存在的.使氢氟酸分子缔合的作用力是氢键.
(3)请根据下表提供的第一电离能数据判断,最有可能生成较稳定的单核阳离子的卤素原子是碘(写出名称).
| 氟 | 氯 | 溴 | 碘 | |
| 第一电离能(kJ/mol) | 1681 | 1251 | 1140 | 1008 |

请比较二者酸性强弱:HIO3> H5IO6(填“>”、“<”或“=”).
(5)硼酸(H3BO3)是一种片层状结构的白色晶体,层内的H3B03分子间通过氢键相连(如图2).则1molH3BO3的晶体中有3 mol氢键.
硼酸溶于水生成弱电解质一水合硼酸B(OH)3•H2 O,它电离生成少量[B(OH)4]一和H+,则[B(OH)4]一含有的化学键类型为共价键、配位键.
(6)如图所示的二维平面晶体示意图3中表示化学式为AX3的是b.
6.化学是材料科学发展的基础.下列说法正确的是( )
| A. | 我们使用合金是因为它比纯金属具有更优良的化学性质 | |
| B. | 钢化玻璃、有机玻璃、防弹玻璃均属于硅酸盐材料 | |
| C. | 高分子材料可能在特殊情况导电,如聚乙炔 | |
| D. | 可用作荧光灯内壁保护层的纳米氧化铝属于胶体 |
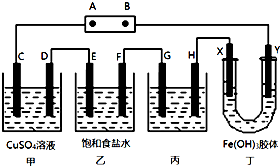 某研究性学习小组将下列装置如图连接,C、D、E、F、X、Y 都是惰性电极.将电源接通后,向乙中滴入酚酞试液,在F极附近显红色.试回答下列问题:
某研究性学习小组将下列装置如图连接,C、D、E、F、X、Y 都是惰性电极.将电源接通后,向乙中滴入酚酞试液,在F极附近显红色.试回答下列问题: