题目内容
有机物A是衡量一个国家石油工业是否发达的标志性物质,A在催化剂作用与水反应的产物为B,B可与食醋中的有机酸C发生反应生成D,下列说法中正确的是( )
| A、实验室制取D时,使用水浴加热 |
| B、A能与溴水和酸性KMnO4溶液发生氧化还原反应,而使它们褪色 |
| C、D的同分异构体中含有羧基的有3种 |
| D、B和C的熔点和沸点都比C2H6、C2H4的沸点和熔点高 |
考点:有机物的推断
专题:有机物的化学性质及推断
分析:有机物A是衡量一个国家石油工业是否发达的标志性物质,则A为CH2=CH2,A在催化剂作用与水反应的产物为B,则B为CH3CH2OH,B可与食醋中的有机酸C发生反应生成D,则C为CH3COOH、D为CH3COOCH2CH3,据此解答.
解答:
解:有机物A是衡量一个国家石油工业是否发达的标志性物质,则A为CH2=CH2,A在催化剂作用与水反应的产物为B,则B为CH3CH2OH,B可与食醋中的有机酸C发生反应生成D,则C为CH3COOH、D为CH3COOCH2CH3,
A.制备乙酸乙酯时,不用水浴加热,采取直接加热,故A错误;
B.A为CH2=CH2,含有碳碳双键,与酸性KMnO4溶液发生氧化还原反应,而与溴水发生加成反应,使它们褪色,故B错误;
C.D为CH3COOCH2CH3,同分异构体中含有羧基有:CH3CH2CH2COOH、(CH3)2CHCOOH,故C错误;
D.B为CH3CH2OH,C为CH3COOH,分子之间存在氢键,常温下为液态,而C2H6、C2H4常温下气体,故乙醇、乙酸的熔点和沸点都比C2H6、C2H4的沸点和熔点高,故D正确,
故选D.
A.制备乙酸乙酯时,不用水浴加热,采取直接加热,故A错误;
B.A为CH2=CH2,含有碳碳双键,与酸性KMnO4溶液发生氧化还原反应,而与溴水发生加成反应,使它们褪色,故B错误;
C.D为CH3COOCH2CH3,同分异构体中含有羧基有:CH3CH2CH2COOH、(CH3)2CHCOOH,故C错误;
D.B为CH3CH2OH,C为CH3COOH,分子之间存在氢键,常温下为液态,而C2H6、C2H4常温下气体,故乙醇、乙酸的熔点和沸点都比C2H6、C2H4的沸点和熔点高,故D正确,
故选D.
点评:本题考查有机物推断、同分异构体、官能团性质等,比较基础,需要学生熟练掌握常见有机物的性质与转化.

练习册系列答案
相关题目
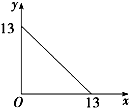 T℃下的溶液中,c(H+)=1.0×10-xmol?L-1,c(OH-)=1.0×10-ymol?L-1,x与y的关系如图所示.下列说法不正确的是( )
T℃下的溶液中,c(H+)=1.0×10-xmol?L-1,c(OH-)=1.0×10-ymol?L-1,x与y的关系如图所示.下列说法不正确的是( )| A、T℃时,水的离子积Kw为1×10-13 |
| B、T>25 |
| C、T℃时,pH=7的溶液显碱性 |
| D、T℃时,pH=12的苛性钠溶液与pH=1的稀硫酸等体积混合,溶液的pH=7 |
已知c(NH4Cl)小于0.1mol/L时,溶液的pH>5.1,现用0.1mol/LHCl滴定10mL0.05mol/L氨水,用甲基橙作指示剂(变色范围为3.1~4.4),达到终点所用盐酸( )
| A、10mL | B、5mL |
| C、大于5mL | D、小于5mL |
某烃完全燃烧生成二氧化碳和水的物质的量之比为1:1,在标准状况下的密度为2.5g/L,其分子式为( )
| A、C2H4 |
| B、C4H8 |
| C、C4H10 |
| D、C5H10 |
 某兴趣小组进行“活泼金属与酸反应”的实验,将5.4g的铝片投入500mL 0.5mol?L-1的硫酸溶液中,右图为反应产生氢气速率与反应时间的关系图.
某兴趣小组进行“活泼金属与酸反应”的实验,将5.4g的铝片投入500mL 0.5mol?L-1的硫酸溶液中,右图为反应产生氢气速率与反应时间的关系图.
 NO3-+
NO3-+ ═
═ Fe2++
Fe2++ NH4++
NH4++