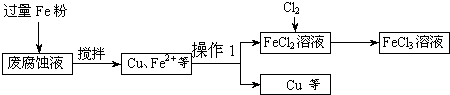
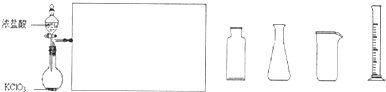
题目内容
|
下列反应中盐酸为氧化剂的是 | |
| [ ] | |
A. |
Zn+2HCl |
B. |
CaCO3+2HCl |
C. |
KClO3+6HCl |
D. |
Ca(ClO)2+2HCl |
答案:A
解析:
解析:
|
本题要求判断盐酸在题给反应中为氧化剂,所以组成HCl的两种元素中,只能是氢元素由+1价降为零价(即有H2生成)才是正确选项. |

练习册系列答案
相关题目
实验室常用强氧化剂(如KMnO4、KClO3、MnO2等)氧化浓盐酸的方法来制备氯气.某研究性学习小组欲探究用Na2O2与浓盐酸制备并检验氯气.供选用的实验试剂及装置如下(部分导管、蒸馏水略):
a、Na2O2 b、浓盐酸 c、碱石灰 d、NaOH溶液 e、淀粉-KI溶液
f、CaCO3g、石蕊试液 h、饱和NaCl溶液
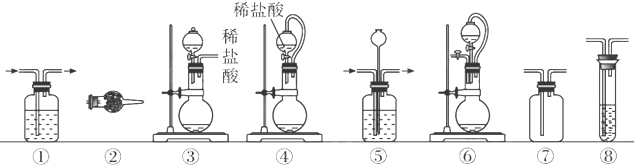
(1)写出实验室用二氧化锰和浓盐酸反应制备氯气的离子方程式
(2)写出用Na2O2与浓盐酸制备氯气的化学方程式 .该反应中盐酸的作用是
(3)下列装置组合最合理的是 (填序号,需考虑实验结束撤除装置时残留有害气体的处理).
(4)尾气经处理后仍有较多气体排出,其主要原因可用化学方程式表示为: .
(5)某小组成员建议用双氧水代替过氧化钠进行实验更好,请你给出两条合适的理由:
① ,
② .
a、Na2O2 b、浓盐酸 c、碱石灰 d、NaOH溶液 e、淀粉-KI溶液
f、CaCO3g、石蕊试液 h、饱和NaCl溶液

(1)写出实验室用二氧化锰和浓盐酸反应制备氯气的离子方程式
(2)写出用Na2O2与浓盐酸制备氯气的化学方程式
(3)下列装置组合最合理的是
| 组合 | 制备装置 | 净化装置 | 检验装置/试剂 | 尾气处理装置 |
| A | ③ | ② | ⑦/e | ⑤ |
| B | ③⑥ | ① | ⑧/g | ① |
| C | ④ | ① | ⑤/e | ② |
| D | ⑥ | ⑤ | ⑧/g | ① |
(5)某小组成员建议用双氧水代替过氧化钠进行实验更好,请你给出两条合适的理由:
①
②