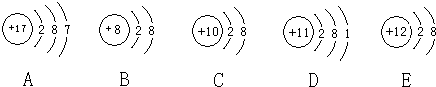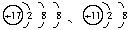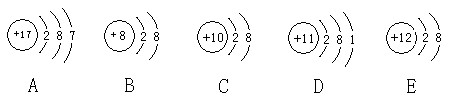��Ŀ����
�۲�����A��B��C��D��E�������ӣ�ԭ�ӻ����ӣ��Ľṹʾ��ͼ���ش��й����⣺

1.�������ӽṹʾ��ͼ���� �� �� �� ����д�����ţ���
2.���������У��������ȶ���ԭ���� �� ������������д���ڱ�С������ͬ����������ʧȥ���ӵ�ԭ���� �������õ����ӵ�ԭ���� ��
3.A��E����Ԫ���γɵĻ�������ˮ��Һ�еĵ��뷽��ʽ�� ����
4.�ں˵����Ϊ1-18��Ԫ���У�д��������B������Ӳ��Ų���ͬ�����ӣ������ӵķ���Ϊ �� �� �� ��A-E���ѳ��ֵ�Ԫ�س��⣩��
5.��һ�������£�D���Ժ͵�����N2�����ϳ�һ�ְ�ɫ���ʣ������ʵĻ�ѧʽ������ ����
1. B E��
2. C D A
3.MgCl2 = Mg2+ + 2Cl-
4. Al3+ F���� ��
5. Na3N
�����������ݽṹʾ��ͼ���ж�A��B��C��D��E�������ֱ���Cl����O2����Ne��Na��
Mg2����
1.�����������ں�������������������ӡ�С���������ӡ�����������ԭ�ӣ����Դ���B��E��
2.�������Ӵﵽ8���ӻ�2�����ȶ��ṹ�ģ������ʾ����ȶ��ģ������������ȶ���ԭ����ϡ������ԭ��Ne���ǽ�����Խǿ��Խ�õ����ӣ�������Խǿ��Խ��ʧȥ���ӣ����Դ𰸷ֱ���Cl��Na��
3.A��E����Ԫ���γɵĻ��������Ȼ�þ���Ȼ�þ�����ӻ�������뷽��ʽΪMgCl2 = Mg2+ + 2Cl-��
4.��B������Ӳ��Ų���ͬ�������������Ӻ�F����
5.�����ڻ��õĽ������ڷ�Ӧ��ʧȥ1�����ӣ��ԣ�1�ۡ���Ԫ���ڷ�Ӧ�еõ�3�����ӣ��ԣ�3�ۣ������ƺ͵�����Ӧ�������ӻ����ﵪ���ƣ���ѧʽΪNa3N