题目内容
某溶液可能含有Cl-、SO42-、CO32-、NH4+、Fe3+、Al3+和K+.取该溶液100mL,加入过量NaOH溶液,加热,得到0.02mol气体,同时产生红褐色沉淀;过滤,洗涤,灼烧,得到0.8g固体;向上述滤液中加足量BaCl2溶液,得到4.66g不溶于盐酸的沉淀.由此可知原溶液中( )
| A、至少存在5种离子 |
| B、Cl-一定存在,且c(Cl-)≥0.1mol/L |
| C、SO42-、NH4+一定存在,Cl-可能不存在 |
| D、CO32-、Al3+一定不存在,K+可能存在 |
考点:物质的检验和鉴别的实验方案设计,常见阳离子的检验,常见阴离子的检验
专题:物质检验鉴别题
分析:加入过量NaOH溶液,加热,得到0.02mol气体,可知一定存在铵离子;
红褐色沉淀是氢氧化铁,0.8g固体为三氧化二铁,其物质的量是可知一定有Fe3+,一定没有CO32-;
4.66g不溶于盐酸的沉淀,硫酸钡沉淀,物质的量为:0.02mol;
根据以上数据推算存在离子,根据电荷守恒推算氯离子的存在及数据.
红褐色沉淀是氢氧化铁,0.8g固体为三氧化二铁,其物质的量是可知一定有Fe3+,一定没有CO32-;
4.66g不溶于盐酸的沉淀,硫酸钡沉淀,物质的量为:0.02mol;
根据以上数据推算存在离子,根据电荷守恒推算氯离子的存在及数据.
解答:
解:由于加入过量NaOH溶液,加热,得到0.02mol气体,说明一定有NH4+,且物质的量为0.02mol;同时产生红褐色沉淀,说明一定有Fe3+,0.8g固体为氧化铁,物质的量为0.005mol,故有0.01molFe3+,一定没有CO32-;4.66g不溶于盐酸的沉淀为硫酸钡,一定有SO42-,物质的量为0.02mol;根K+可能存在,据电荷守恒,一定有Cl-,至少 0.01mol×3+0.02-0.02mol×2=0.01mol,物质的量浓度至少
=0.1mol/L,
A、至少存在Cl-、SO42-、NH4+、Fe3+四种离子,故A错误;
B、Cl-一定存在,根据电荷守恒,至少存在0.01molCl-,有钾离子,氯离子的量会增多.所以c(Cl-)≥0.1mol/L故B正确;
C、一定存在氯离子,故C错误;
D、Al3+无法判断是否存在,K+可能存在,故D错误;
故选B.
| 0.01mol |
| 0.1L |
A、至少存在Cl-、SO42-、NH4+、Fe3+四种离子,故A错误;
B、Cl-一定存在,根据电荷守恒,至少存在0.01molCl-,有钾离子,氯离子的量会增多.所以c(Cl-)≥0.1mol/L故B正确;
C、一定存在氯离子,故C错误;
D、Al3+无法判断是否存在,K+可能存在,故D错误;
故选B.
点评:本题考查离子共存知识,做题是认真阅读、分析题中数据,合理分析,特别是氯离子的推断,难度中等.

练习册系列答案
相关题目
下列有机化合物中的所有碳原子能处于同一平面上的是( )
| A、CH3CH2CH2CH2CH2CH3 |
B、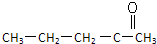 |
| C、CH2═CH-CH═CH2 |
| D、(CH3)3C-C≡C-CH=CHCH3CH2 |
摩尔是( )
| A、国际单位制的一个基本物理量 |
| B、表示物质质量的单位 |
| C、计量微观粒子的物质的量的单位 |
| D、表示6.02×1023个粒子的集体 |
把铜粉放入装有浓氨水的试管中,塞紧试管塞,振荡后发现试管塞越来越紧,且溶液逐渐变为浅黄色(近乎无色)溶液,打开试管塞后,溶液迅速变为蓝色溶液.则下列说法不正确的是( )
| A、试管塞越来越紧,是因为反应消耗了大量O2 |
| B、打开试管塞前Cu元素的化合价为+1价 |
| C、溶液迅速变为蓝色溶液,是因为反应生成了[Cu(H2O)4]2+ |
| D、上述反应原理可用于测定O2的含量 |
 铈、铬、钴、镍虽不是中学阶段常见的金属元素,但在工业生产中有着重要作用.
铈、铬、钴、镍虽不是中学阶段常见的金属元素,但在工业生产中有着重要作用.