题目内容
下列化学用语表述正确的是( )
| A、碳酸溶于水的电离方程式:H2CO3?CO32-+2H+ |
| B、标准状况下将112mL Cl2通入10 mL 1 mol?L-1 FeBr2溶液的离子方程式:2Fe2++4Br-+3Cl2=2Fe3++6Cl-+2Br2 |
C、用单线桥表示浓盐酸和KClO3反应的电子转移的数目与方向: |
D、过氧化钠的电子式为: |
考点:离子方程式的书写,电离方程式的书写,球棍模型与比例模型,用电子式表示简单的离子化合物和共价化合物的形成
专题:化学用语专题
分析:A.碳酸为二元弱酸,其电离过程分步进行,主要以第一步电离为主;
B.亚铁离子还原性大于溴离子,亚铁离子优先与氯气反应,先判断过量情况,然后判断离子方程式正误;
C.氯酸钾中+5价的氯原子被还原成0价的氯气,反应中转移了5个电子;
D.过氧化钠为离子化合物,钠离子直接用离子符号表示,过氧根离子需要标出所带电荷及最外层电子.
B.亚铁离子还原性大于溴离子,亚铁离子优先与氯气反应,先判断过量情况,然后判断离子方程式正误;
C.氯酸钾中+5价的氯原子被还原成0价的氯气,反应中转移了5个电子;
D.过氧化钠为离子化合物,钠离子直接用离子符号表示,过氧根离子需要标出所带电荷及最外层电子.
解答:
解:A.碳酸的电离分步进行,其电离方程式主要写出第一步即可,正确的电离方程式为:H2CO3?HCO3-+H+,故A错误;
B.标准状况下将112mL Cl2的物质的量为0.005mol,10mL 1mol?L-1 FeBr2溶液中含有溴化亚铁0.01mol,含有0.01mol亚铁离子、0.02mol溴离子,由于亚铁离子还原性大于溴离子,亚铁离子优先被氯气氧化,0.01mol亚铁离子完全被氧化需要消耗0.005mol氯气,则氯气完全反应,溴离子没有被氧化,正确的离子方程式为:2Fe2++Cl2=2Fe3++2Cl-,故C错误;
C.反应方程式KClO3+6HCl═KCl+3Cl2↑+3H2O中,KClO3中Cl元素化合价由+5价变成0价,化合价降低5价,HCl中氯元素化合价由-1价升高为0价,化合价升高1价,用单线桥表示方程式中标出电子转移的方向和数目为: ,故C错误;
,故C错误;
D.过氧化钠属于离子化合物,过氧化钠中存在钠离子和过氧根离子,阴阳离子都需要标出所带电荷,过氧化钠的电子式为: ,故D正确;
,故D正确;
故选D.
B.标准状况下将112mL Cl2的物质的量为0.005mol,10mL 1mol?L-1 FeBr2溶液中含有溴化亚铁0.01mol,含有0.01mol亚铁离子、0.02mol溴离子,由于亚铁离子还原性大于溴离子,亚铁离子优先被氯气氧化,0.01mol亚铁离子完全被氧化需要消耗0.005mol氯气,则氯气完全反应,溴离子没有被氧化,正确的离子方程式为:2Fe2++Cl2=2Fe3++2Cl-,故C错误;
C.反应方程式KClO3+6HCl═KCl+3Cl2↑+3H2O中,KClO3中Cl元素化合价由+5价变成0价,化合价降低5价,HCl中氯元素化合价由-1价升高为0价,化合价升高1价,用单线桥表示方程式中标出电子转移的方向和数目为:
 ,故C错误;
,故C错误;D.过氧化钠属于离子化合物,过氧化钠中存在钠离子和过氧根离子,阴阳离子都需要标出所带电荷,过氧化钠的电子式为:
 ,故D正确;
,故D正确;故选D.
点评:本题考查了离子方程式、电子式的书写判断,氧化还原反应中电子转移的表示方法,属于中等难度的试题,注意掌握离子方程式、电子式的书写原则,明确氧化还原反应中电子转移的表示方法.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 16、下列模型分别是HCN、S8、SF6、B12结构单元,下列说法错误的是( )
16、下列模型分别是HCN、S8、SF6、B12结构单元,下列说法错误的是( )| A、已知单质硼的结构单元是由20个正三角形构成的正二十面体,则这个结构单元中含有30个B-B键、12个硼原子 |
| B、SF6的分子空间构型为正八面体 |
| C、1 molHCN分子中有2 molσ键和2molπ键 |
| D、32gS8分子中含有0.125 molσ键 |
下列条件的变化,是因为降低反应所需的能量而增加单位体积内的反应物活化分子百分数致使反应速率加快的是( )
| A、增大浓度 | B、增大压强 |
| C、升高温度 | D、使用催化剂 |
a g H2O中含有b个氧原子,则阿伏伽德罗常数为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
下列水解的离子方程式正确的是( )
| A、S2-+2H2O?H2S+2OH- |
| B、Fe3++3H2O?Fe(OH)3+3H+ |
| C、CO32-+H2O?HCO3-+OH- |
| D、HS-+H2O?H2S↑+OH- |
药物贝诺酯可由乙酰水杨酸和对乙酰氨基酚在一定条件下反应制得:
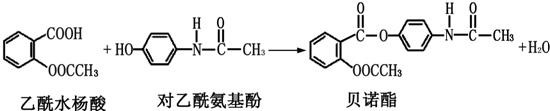
有关上述反应物和产物的叙述正确的是( )

有关上述反应物和产物的叙述正确的是( )
| A、上述反应类型为取代反应 |
| B、按碳的骨架分类,上述三种有机物均属于芳香烃 |
| C、1mol乙酰水杨酸最多能与含2mol NaOH的水溶液发生反应 |
| D、贝诺酯分子中有三种不同类型的含氧官能团 |