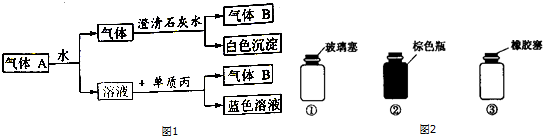
题目内容
17.如图甲是课本中验证铜和浓硝酸反应的装置,乙、丙是师生对演示实验改进后的装置: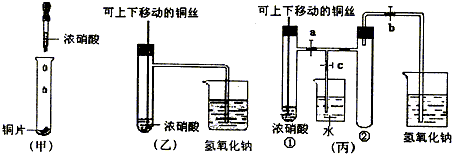
(1)写出铜和浓硝酸反应的离子方程式Cu+4H++2NO3-=Cu2++2NO2↑+2H2O.
(2)和甲装置相比,乙装置的优点有 ①可以控制反应;②吸收NO2气体,防止污染环境.
(3)为了进一步验证NO2和水的反应,某学生设计了丙装置,做实验时先关闭弹簧夹c,
(填a、b、c,下同),再打开弹簧夹a、b,才能使NO2气体充满②试管.当气体充满②试管后,将铜丝提起与溶液脱离,欲使烧杯中的水进入②试管,应进行的操作是先关闭b,再关闭a,然后打开c,用手捂住(热水、热毛巾、加热)试管②.
(4)②试管中的NO2和水充分反应后,所得溶液物质的量浓度的最大值是0.045mol•L-1(气体体积按标准状况计算).
分析 (1)根据铜和浓硝酸反应生成硝酸铜、二氧化氮和水;
(2)根据反应可控制,随时可以停止;根据反应无污染物
(3)根据此步骤是为了NO2气体充满②试管;让二氧化氮与水接触发生反应;
(4)根据NO2和水反应,设试管的容积为VL,求出溶质的物质的量及溶液的体积;
解答 解:(1)因铜和浓硝酸反应生成硝酸铜、二氧化氮和水,故答案为:Cu+4H++2NO3-=Cu2++2NO2↑+2H2O;
(2)乙装置能使反应可控制,随时可以停止,同时吸收NO2气体,防止污染环境,
故答案为:①可以控制反应②吸收NO2气体,防止污染环境;
(3)为了NO2气体充满②试管,应先关闭c,然后打开a、b,为了让二氧化氮与水接触发生反,应先关闭b,再关闭a,然后打开c,用手捂住(热水、热毛巾、加热)试管②,故答案为:c;a、b;先关闭b,再关闭a,然后打开c,用手捂住(热水、热毛巾、加热)试管②;
(4)设试管的容积为VL,根据NO2和水反应:3NO2 +H2O=2HNO3 +NO
$\frac{V}{22.4}$ $\frac{V}{22.4}$×$\frac{2}{3}$
反应后溶液中的溶质HNO3的物质的量为 $\frac{V}{22.4}$×$\frac{2}{3}$mol,溶液的体积为V×$\frac{2}{3}$L,
所以溶液物质的量浓度为:$\frac{1}{22.4}$mol•L-1=0.045mol•L-1,
故答案为:0.045mol•L-1.
点评 本题主要考查了铜和浓硝酸的反应,同时考查了溶液浓度的计算,培养了学生计算能力.

| A. | Na | B. | Mg | C. | Al | D. | Si |
| A. | 福尔马林可作食品的保鲜剂 | |
| B. | 乙烯可作水果的催熟剂 | |
| C. | 做衣服的棉和麻均与淀粉互为同分异构体 | |
| D. | 磨豆浆的大豆富含蛋白质,豆浆煮沸后蛋白质变成了氨基酸 |
| A. | Cl2的化学性质活泼,与H2混合后立刻发生爆炸 | |
| B. | 新制的氯水光照会产生气泡,该气体是Cl2 | |
| C. | 若发生Cl2泄露,应立即向上风地区转移 | |
| D. | 漂白粉比HClO稳定,可露置在空气中长期保存且不影响使用效果 |
| A. | 乙炔分子的比例模型示意图: | B. | 溴乙烷的电子式: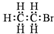 | ||
| C. | 1,3-丁二烯的分子式:C4H8 | D. | 乙醇的结构简式:CH3CH2OH |
a.HOCH2CH2CH2OH
b.CH3CH2COOCH3
c.CH3CH2CH2OH
d.HOCH2CH(OH)CH2OH.
| A. | b<c<a<d | B. | a<b<c<d | C. | d<a<b<c | D. | c<d<b<a |