题目内容
9.2015年12月杭州多日被雾霾笼罩,有报道称雾霾颗粒中汽车尾气占20%以上.已知汽车尾气中的主要污染物为NOx、CO、燃烧源超细颗粒(PM2.5)等有害物质.目前,已研究出了多种消除汽车尾气污染的方法.Ⅰ.在汽车尾气系统中装置催化转化器,可有效降低NOX的排放.已知:
N2(g)+O2(g)═2NO(g)△H=+180.5kJ•mol-1
2C(s)+O2(g)═2CO(g)△H=-221.0kJ•mol-1
C(s)+O2(g)═CO2(g)△H=-393.5kJ•mol-1
(1)NOx能形成酸雨,写出NO2转化为HNO3的化学方程式:4NO2+O2+2H2O═4HNO3.
(2)尾气转化的反应之一:2NO(g)+2CO(g)═N2(g)+2CO2(g)△H=-746.5KJ/mol.
(3)已知:N2、O2分子中化学键的键能分别是946kJ•mol-1、497kJ•mol-1,则NO分子中化学键的键能为631.5kJ•mol-1.
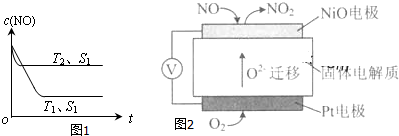
(4)当质量一定时,增大固体催化剂的表面积可提高化学反应速率.如图1表示在其他条件不变时,反应:2NO(g)+2CO(g)?2CO2(g)+N2(g) 中NO的浓度[c(NO)]随温度(T)、催化剂表面积(S)和时间(t)的变化曲线.若催化剂的表面积S1>S2,在图1中画出c(NO) 在T1、S2条件下达到平衡过程中的变化曲线.
Ⅱ.还原法.用活性炭还原法处理氮氧化物.有关反应为:C(s)+2NO(g)?N2(g)+CO2(g)△H.某研究小组向某密闭容器加入一定量的活性炭和NO,恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
浓度/mol•L-1 时间/min | NO | N2 | CO2 |
| 0 | 0.100 | 0 | 0 |
| 10 | 0.058 | 0.021 | 0.021 |
| 20 | 0.040 | 0.030 | 0.030 |
| 30 | 0.040 | 0.030 | 0.030 |
| 40 | 0.032 | 0.034 | 0.017 |
| 50 | 0.032 | 0.034 | 0.017 |
(2)30min后,改变某一条件,反应重新达到平衡,则改变的条件可能是减小CO2的浓度.
(3)若30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为 5:3:3,则该反应的△H<0(填“>”、“=”或“<”).
Ⅲ.变废为宝.
(1)CO可用于合成CH3OH,反应方程式为:CO(g)+2H2(g)?CH3OH(g),在一定温度压强下(甲醇为气体),在容积为2L的密闭容器中通入0.2molCO与0.4molH2,达平衡时CO的转化率50%,再加入1.0molCO后重新达到平衡,则CO的转化率减小(填“增大”、“不变”或“减小”);
(2)通过NOx传感器可监测NOx的含量,其工作原理示意图如图2:
①Pt电极上发生的是还原反应(填“氧化”或“还原”).
②写出NiO电极的电极反应式:NO+O2--2e-=NO2.
分析 Ⅰ.(1)二氧化氮和氧气按照4:1溶于水全部生成硝酸;
(2)①N2(g)+O2(g)═2NO(g)△H=+180.5kJ•mol-1
②2C(s)+O2(g)═2CO(g)△H=-221.0kJ•mol-1
③C(s)+O2(g)═CO2(g)△H=-393.5kJ•mol-1
依据盖斯定律计算③×2-②-①得到热化学方程式;
(3)据△H=反应物键能和-生成物键能和求算;
(4)催化剂的表面积S1>S2,则催化剂S1到达平衡的时间比催化剂S2短,催化剂不影响平衡移动,平衡时NO的浓度相同,据此作图;
Ⅱ.(1)依据图表数据结合化学平衡常数概念是利用生成物平衡浓度幂次方乘积除以反应物平衡浓度幂次方乘积计算得到;
(2)依据图表数据计算分析判断,化学平衡常数随温度变化,平衡常数不变说明改变的条件一定不是温度;依据数据分析,氮气浓度增大,二氧化碳和一氧化氮浓度减小;
(3)依据平衡浓度之比和30min前达到的平衡浓度比较分析平衡移动方向,结合平衡移动原理判断反应热量变化;
Ⅲ.(1)CO转化率为50%,CO(g)+2H2(g)?CH3OH(g)
初始浓度(mol/L):0.1 0.2 0
变化浓度(mol/L):0.05 0.1 0.05
平衡浓度(mol/L):0.05 0.1 0.05
则该温度下的平衡常数为 $\frac{0.05}{0.05×0.{1}^{2}}$=100,
再加入1.0mol CO后,可采用极限法计算,假设H2完全转化,则
CO(g)+2H2(g)?CH3OH(g)
初始浓度(mol/L):0.6 0.2 0
变化浓度(mol/L):0.1 0.2 0.1
平衡浓度(mol/L):0.5 0 0.1
计算一氧化碳转化率判断;
(2)①得电子的物质发生还原反应;
②NiO电极上NO失电子和氧离子反应生成二氧化氮.
解答 解:Ⅰ.(1)NOx能形成酸雨,NO2转化为HNO3的总反应的化学方程式为:4NO2+O2+2H2O═4HNO3,故答案为:4NO2+O2+2H2O═4HNO3;
(2)①N2(g)+O2(g)═2NO(g)△H=+180.5kJ•mol-1
②2C(s)+O2(g)═2CO(g)△H=-221.0kJ•mol-1
③C(s)+O2(g)═CO2(g)△H=-393.5kJ•mol-1
依据盖斯定律计算③×2-②-①得到热化学方程式2NO(g)+2CO(g)═N2(g)+2CO2(g)△H=-746.5KJ/mol,
故答案为:-746.5KJ/mol;
(3)△H=反应物键能和-生成物键能和,946kJ/mol+497kJ/mol-2Q(N-O)=180.0kJ/mol,Q(N-O)=631.5KJ/mol,故答案为:631.5;
(4)催化剂的表面积S1>S2,则催化剂S1到达平衡的时间比催化剂S2短,催化剂不影响平衡移动,平衡时NO的浓度相同,故c(NO) 在T1、S2条件下达到平衡过程中的变化曲线为: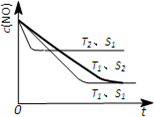 ,故答案为:
,故答案为: .
.
Ⅱ.(1)平衡状态物质的平衡浓度为,c(NO)=0.04mol/L;c(N2)=0.03mol/L;c(CO2)=0.03mol/L;K=$\frac{c({N}_{2})c(C{O}_{2})}{{c}^{2}(NO)}$=$\frac{0.03×0.03}{0.0{4}^{2}}$=0.56;
故答案为:0.56;
(2)30min时改变某一条件,反应重新达到平衡,依据平衡常数计算得到c(N2)=0.034mol/L;c(CO2)=0.017mol/L;c(NO)=0.032mol/L;K=$\frac{c({N}_{2})c(C{O}_{2})}{{c}^{2}(NO)}$=$\frac{0.034×0.017}{0.03{2}^{2}}$=0.56,化学平衡常数随温度变化,平衡常数不变说明改变的条件一定不是温度;依据数据分析,氮气浓度增大,二氧化碳和一氧化氮浓度减小,反应前后气体体积不变,所以可能是减小二氧化碳浓度,
故答案为:减小CO2的浓度;
(3)若30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为5:3:3,和图表数据分析判断,平衡逆向进行,由平衡移动原理可知,升温平衡向吸热反应方向进行,所以正反应为放热反应;反应的△H<0;
故答案为:<;
Ⅲ.(1)CO转化率为50%,CO(g)+2H2(g)?CH3OH(g)
初始浓度(mol/L):0.1 0.2 0
变化浓度(mol/L):0.05 0.1 0.05
平衡浓度(mol/L):0.05 0.1 0.05
则该温度下的平衡常数为 $\frac{0.05}{0.05×0.{1}^{2}}$=100,
再加入1.0mol CO后,可采用极限法计算,假设H2完全转化,则
CO(g)+2H2(g)?CH3OH(g)
初始浓度(mol/L):0.6 0.2 0
变化浓度(mol/L):0.1 0.2 0.1
平衡浓度(mol/L):0.5 0 0.1
则重新达到平衡,CO的转化率 $\frac{0.1}{0.6}$×100%=$\frac{1}{6}$<50%,则转化率减小,
故答案为:减小;
(2)①铂电极上氧气得电子生成氧离子而被还原,故答案为:还原;
②NiO电极上NO失电子和氧离子反应生成二氧化氮,所以电极反应式为:NO+O2--2e-=NO2,故答案为:NO+O2--2e-=NO2.
点评 本题主要考查化学反应速率、影响化学平衡的因素、化学平衡图象、电极反应式的以及热化学方程式的书写等,注意根据“先拐先平数值大”原则判断温度高低是关键,作图时注意到达平衡的时间与平衡时NO的浓度,题目难度中等.

 一本好题口算题卡系列答案
一本好题口算题卡系列答案| A. | 蒸发操作时,应使混合物中的水完全蒸干后,才能停止加热 | |
| B. | 蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 | |
| C. | 分液操作时,分液漏斗中的下层液体从下口流出,上层液体从上口倒出 | |
| D. | 萃取操作时,溶质在萃取剂中的溶解度应大于在原溶剂中的溶解度 |
| A. | H20分子中只含有非极性共价键 | |
| B. | H20分子中只含有极性共价键 | |
| C. | 水分子间只存在氢键 | |
| D. | 冷却反应堆用水在地球上常温下是固态 |
| A. | 常温常压下,28g CO和N2的混合物含有的分子数为 NA | |
| B. | 标准状况下,1mol氦气中含有的核外电子数为4NA | |
| C. | 标准状况下,22.4 L 苯中含有的苯分子数是NA | |
| D. | 常温常压下,0.10 mol•L-1CH3COOH溶液中含有的H+数小于0.1NA |
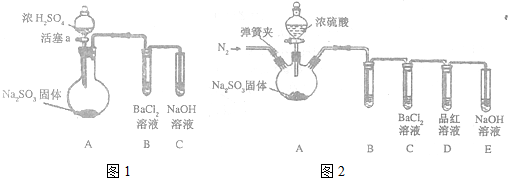

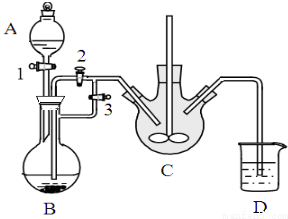 乳酸亚铁([CH3CH(OH)COO]2Fe•3H2O,M=288g/mol)是一种常用的补铁剂,可通过乳酸与碳酸亚铁反应制得:CH3CH(OH)COOH+FeCO3+2H2O→[CH3CH(OH)COO]2Fe•3H2O+CO2↑.
乳酸亚铁([CH3CH(OH)COO]2Fe•3H2O,M=288g/mol)是一种常用的补铁剂,可通过乳酸与碳酸亚铁反应制得:CH3CH(OH)COOH+FeCO3+2H2O→[CH3CH(OH)COO]2Fe•3H2O+CO2↑.