题目内容
3.对0.10mol/L的碳酸钠溶液加热,利用传感器测定溶液的pH,结果如图所示,下列对实验结果的分析不正确的是( )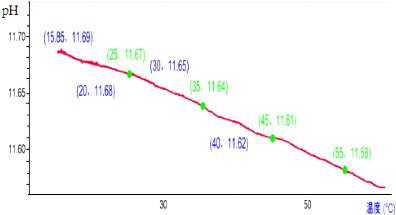
| A. | 随着温度升高溶液中c(OH-)不断减小 | |
| B. | 加热促进CO32-水解和水的电离,溶液中c(OH-)随温度升高而增大 | |
| C. | 溶液pH减小的原因是:加热促进水的电离,Kw随温度升高而增大 | |
| D. | 25℃时CO32-的水解程度约为100.67% |
分析 A.加热碳酸钠溶液,溶液pH受温度影响,加热促进CO32-水解;
B.加热促进水的电离,Kw增大;
C..由图象分析,引起溶液pH减小的原因是Kw增大所导致;
D.25°C时PH=11.63,溶液中c(OH-)=10-2.33 mol/L,水解的碳酸根离子浓度除以原来浓度计算得到水解度.
解答 解:A.加热碳酸钠溶液,溶液pH受温度影响,加热促进CO32-水解,溶液中c(OH-)增大,故A错误;
B.加热促进水的电离,Kw增大.根据溶液pH=pKw-pOH可知:溶液中的c(OH-)随温度升高而增大,故B正确;
C.由实验结果分析,引起溶液pH减小的原因是Kw,加热促进水的电离,Kw增大,故C正确;
D.25℃时PH=11.63,溶液中c(OH-)=10-2.33 mol/L,CO32-的水解度≈$\frac{1{0}^{-2.33}mol/L}{0.10mol/L}$×100%=100.67%,故D正确;
故选A.
点评 本题考查了盐类水解原理、水解过程中溶液PH计算,离子积常数的分析应用,掌握基础是解题关键,题目难度中等.

练习册系列答案
 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案
相关题目
12.下列各组中的两种物质在溶液中的反应,可用同一种离子方程式表示的是( )
| A. | 氧化铜分别溶于盐酸和醋酸 | |
| B. | 石灰石分别与硝酸和盐酸反应 | |
| C. | 硫酸铜溶液分别与氯化钡和氢氧化钡溶液反应 | |
| D. | 稀硫酸分别与碳酸钠、碳酸氢钠溶液反应 |
10.下列化学反应中有电子得失的是( )
| A. | S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2 | B. | N2+3H2$?_{催化剂}^{高温、高压}$2NH3 | ||
| C. | Mg+Cl2$\frac{\underline{\;点燃\;}}{\;}$MgCl2 | D. | NaHCO3+HCl=NaCl+CO2↑+H2O |
17.有关颜色变化与氧化还原反应有关的是( )
| A. | 苯使溴水褪色 | |
| B. | 长时间放置的KI溶液变棕色 | |
| C. | 将Na2CO3溶液点在红色石蕊试纸上,试纸变蓝 | |
| D. | 向KSCN与FeCl3的混合溶液中加入FeCl3晶体,溶液颜色加深 |
8.近年来,由于石油价格不断上涨,以煤为原料制备一些化工产品的前景又被看好.如图是以烃A为原料生产人造羊毛的合成路线.下列说法正确的是( )
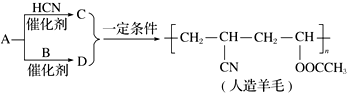

| A. | 合成人造羊毛的反应属于缩聚反应 | B. | A生成C的反应属于加成反应 | ||
| C. | A生成D的反应属于取代反应 | D. | 烃A的结构简式为CH2═CH2 |
15.下列分子的立体结构模型正确的是( )
| A. | CO2的立体结构模型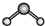 | B. | PH3的立体结构模型 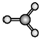 | ||
| C. | H2S的立体结构模型 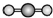 | D. | CH4的立体结构模型 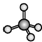 |
13.下列说法中正确的是( )
| A. | Na在空气中缓慢氧化生成白色的Na2O2 | |
| B. | Na在空气中燃烧生成淡黄色的Na2O2 | |
| C. | Na在空气中燃烧生成淡黄色的Na2O | |
| D. | Na在空气中燃烧生成白色的Na2O2 |
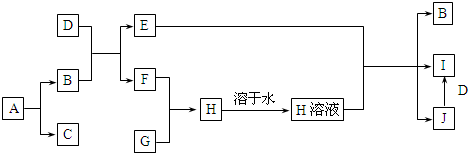 请回答下列问题:
请回答下列问题: