题目内容
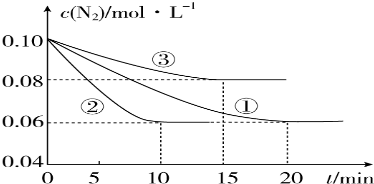
5.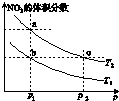 在密闭容器中充入一定量的NO2,发生反应2NO2(g)?N2O4(g)△H=-57kJ•mol-1.在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如图所示.下列说法正确的是( )
在密闭容器中充入一定量的NO2,发生反应2NO2(g)?N2O4(g)△H=-57kJ•mol-1.在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如图所示.下列说法正确的是( )| A. | a、c两点的反应速率:a>c | B. | 由a点到b点,可以用加热的方法 | ||
| C. | a、c两点气体的颜色:a深,c浅 | D. | a、b两点NO2的转化率:a<b |
分析 A.a、c两点的温度相同,压强越大,反应速率越大;
B.该反应为放热反应,压强相同时二氧化氮的体积分数越大,温度越高;
C.a到c点,压强增大,则容器容积减小,则二氧化氮浓度增大,气体颜色加深;
D.a、b的压强相同,二氧化氮的体积分数越大,则二氧化氮的转化率越低.
解答 解:A.a、c两点的温度都是T2,c点压强较大,则反应速率:a<c,故A错误;
B.压强都为p1时,T2时NO2的体积分数较大,结合该反应为放热反应可知温度T1<T2,所以由a点到b点应该用降温的方法,故B错误;
C.a、c两点的温度都是T2,压强增大,说明容器容积缩小,达到平衡时二氧化氮的浓度与原平衡相比增大了,则a、c两点气体的颜色:a浅,c深,故C错误;
D.根据图示可知,a、b两点的压强都为p1,而a点NO2的体积分数较大,则a点二氧化氮转化率减小,所以a、b两点二氧化氮的转化率:a<b,故D正确;
故选D.
点评 本题考查了化学平衡及其影响,题目难度中等,根据图象曲线变化正确判断温度T1、T2的大小为解答根据,注意掌握化学平衡及其影响,试题培养了学生的分析、理解能力及灵活应用能力.

练习册系列答案
 小学课时特训系列答案
小学课时特训系列答案
相关题目
12.反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示,下列说法正确的是( )
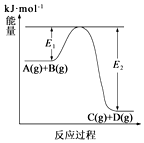

| A. | 上述反应为吸热反应 | B. | 上述反应的△H=E1kJ•mol-1 | ||
| C. | A(g)的能量一定大于C(g) | D. | 反应物的总焓大于反应产物的总焓 |
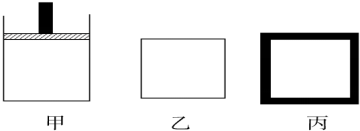
13.下列实验装置、操作不能达到实验目的是( )
| A. | 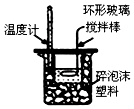 测定中和热 | B. | 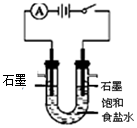 电解食盐水 | ||
| C. | 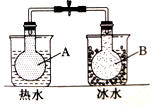 温度对化学平衡的影响 | D. | 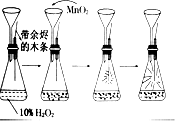 催化剂对反应速率的影响 |
13.某烧碱溶液中含有少量杂质(不与盐酸反应),用标准液盐酸滴定氢氧化钠,测定其浓度.
(1)滴定:用酸式滴定管盛装c mol/L盐酸标准液.实验中选用酚酞作指示剂,当滴入最后一滴盐酸时,溶液由红色变为无色、且半分钟内不变色现象时表示滴定达到终点.实验有关数据记录如下:
(2)根据所给数据,写出计算烧碱样品的物质的量浓度的表达式(不必化简)c=$\frac{\frac{25.30mL+25.35,mL}{2}×1{0}^{-3}L×cmol/L}{V×1{0}^{-3}L}$.
(3)对下列几种假定情况进行讨论:(填“无影响”、“偏高”、“偏低”)
a.若滴定前用蒸馏水冲洗锥形瓶,则会使测定结果无影响;
b.读数时,若滴定前仰视,滴定后俯视,则会使测定结果偏低;
c.若在滴定过程中不慎将数滴酸液滴在锥形瓶外,则会使测定结果偏高;
d.滴加盐酸速度过快,未充分振荡,刚看到溶液变色,立刻停止滴定,则会使测定结果偏低.
(1)滴定:用酸式滴定管盛装c mol/L盐酸标准液.实验中选用酚酞作指示剂,当滴入最后一滴盐酸时,溶液由红色变为无色、且半分钟内不变色现象时表示滴定达到终点.实验有关数据记录如下:
| 滴定 序号 | 待测液体积(mL) | 所消耗盐酸标准液的体积(mL) | ||
| 滴定前 | 滴定后 | 消耗的体积 | ||
| 1 | V | 0.50 | 25.80 | 25.30 |
| 2 | V | 6.00 | 31.35 | 25.35 |
(3)对下列几种假定情况进行讨论:(填“无影响”、“偏高”、“偏低”)
a.若滴定前用蒸馏水冲洗锥形瓶,则会使测定结果无影响;
b.读数时,若滴定前仰视,滴定后俯视,则会使测定结果偏低;
c.若在滴定过程中不慎将数滴酸液滴在锥形瓶外,则会使测定结果偏高;
d.滴加盐酸速度过快,未充分振荡,刚看到溶液变色,立刻停止滴定,则会使测定结果偏低.
14.一定温度下可逆反应:A(s)+2B(g)?2C(g)+D(g);△H>0.现将1molA和2molB加入甲容器中,将4mol C和2mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t1时两容器内均达到平衡状态(如图1所示,隔板K不能移动).下列说法正确的是( )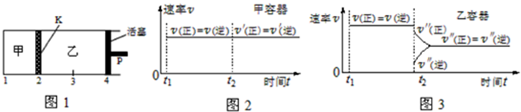

| A. | 保持温度和活塞位置不变,在甲中再加入1 mol A和2 mol B,达到新的平衡后,甲中C的浓度是乙中 C的浓度的2倍 | |
| B. | 保持活塞位置不变,升高温度,达到新的平衡后,甲、乙中B的体积分数均增加 | |
| C. | 保持温度不变,移动活塞P,使乙的容积和甲相等,达到新的平衡后,乙中C的体积分数是甲中C的体积分数的2倍 | |
| D. | 保持温度和乙中的压强不变,t2时分别向甲、乙中加入等质量的氦气后,甲、乙中反应速率变化情况分别如图2和图3所示(t1前的反应速率变化已省略) |
15.常温下,下列有关溶液pH的相关说法正确的是( )
| A. | 将pH=11的氢氧化钠溶液加水稀释100倍,溶液中c(H+)=10-13 mol•L-1 | |
| B. | 将pH=9的氢氧化钠溶液和pH=13的氢氧化钡溶液等体积混合,所得混合溶液的pH=11 | |
| C. | 将pH=13的氢氧化钡溶液和pH=1的盐酸等体积混合,由于氢氧化钡过量,所得溶液的pH>7 | |
| D. | 将pH=1的硫酸和pH=5的盐酸等体积混合,所得混合溶液的pH=1.3 |