题目内容
 实验室需要0.Imol/LNaOH溶液450mL和0.5mol/L硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题:
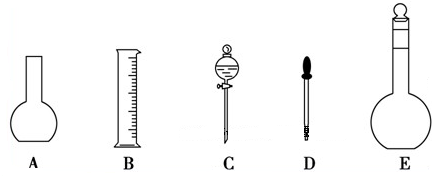
实验室需要0.Imol/LNaOH溶液450mL和0.5mol/L硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题:(1)如图所示的仪器中配制溶液肯定不需要的是
(2)下列操作中,容量瓶所不具备的功能有
A.配制一定体积准确浓度的标准溶液 B.贮存溶液
C.测量容量瓶规格以下的任意体积的液体 D.准确稀释某一浓度的溶液
E.用来加热溶解固体溶质
(3)根据计算用托盘天平称取NaOH的质量为
A.用30mL水洗涤烧杯2-3次,洗涤液均注入容量瓶
B.准确称取计算量的氢氧化钠固体于烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其充分溶解
C.将溶解的氢氧化钠溶液沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度2~3cm处
(4)根据计算得知,所需质量分数为98%、密度为1.84g/cm3的浓硫酸的体积为:
考点:配制一定物质的量浓度的溶液
专题:实验题
分析:(1)根据溶液的配制步骤结合各仪器的构造及使用方法进行判断;
(2)根据容量瓶的构造及正确使用方法进行解答;
(3)实验室没有450mL容量瓶,需要选用500mL容量瓶,实际上配制的溶液为500mL 0.1mol/L的氢氧化钠溶液,根据n=cV计算出氢氧化钠的物质的量,再根据m=nM计算出氢氧化钠的质量;根据配制一定物质的量浓度的溶液步骤对各操作进行排序;
(4)根据c=
计算出浓硫酸的浓度,再根据溶液的稀释过程中溶质的物质的量不变计算出需要浓硫酸的体积,根据计算结果选用量筒规格.
(2)根据容量瓶的构造及正确使用方法进行解答;
(3)实验室没有450mL容量瓶,需要选用500mL容量瓶,实际上配制的溶液为500mL 0.1mol/L的氢氧化钠溶液,根据n=cV计算出氢氧化钠的物质的量,再根据m=nM计算出氢氧化钠的质量;根据配制一定物质的量浓度的溶液步骤对各操作进行排序;
(4)根据c=
| 1000ρw |
| M |
解答:
解:(1)A为平底烧瓶、C为分液漏斗,在配制一定浓度的溶液中不会用到烧瓶和分液漏斗;配制一定物质的量浓度的溶液需要的仪器有:托盘天平、量筒、烧杯、玻璃棒、容量瓶、胶头滴管等,还缺少的玻璃仪器为:烧杯和玻璃棒,
故答案为:AC;烧杯、玻璃棒;
(2)A.容量瓶为定容仪器,用于配制一定体积的、浓度准确的溶液,故A正确;
B.容量瓶只能用来配制一定体积准确浓度的溶液,不能用于贮存溶液,故B错误;
C.容量瓶不能配制或测量容量瓶规格以下的任意体积的液体,故C错误;
D.容量瓶能准确稀释某一浓度的溶液,故D正确;
E.容量瓶只能用于配制一定浓度的溶液,不能用来加热溶解固体溶质,故E错误;
故答案为:BCE;
(3)需要0.1mol/LNaOH溶液450mL,需要配制500mL 0.1mol/L的氢氧化钠溶液,需要氢氧化钠的物质的量为:0.1mol/L×0.5L=0.05mol,需要氢氧化钠的质量为:40g/mol×0.05mol=2.0g;配制500mL 0.1mol/L的氢氧化钠溶液的步骤为:计算、称量、溶解、冷却、移液、洗涤、定容、摇匀等,所以正确的配制顺序为:BCAFED,
故答案为:2.0;BCAFED;
(4)98%、密度为1.84g/cm3的浓硫酸的物质的量浓度为:
mol/L=18.4mol/L,配制0.5mol/L硫酸溶液500mL,需要改浓硫酸的体积为:
≈0.0136L=13.6mL;量取13.6mL浓硫酸,需要使用15mL量筒,
故答案为:13.6;15.
故答案为:AC;烧杯、玻璃棒;
(2)A.容量瓶为定容仪器,用于配制一定体积的、浓度准确的溶液,故A正确;
B.容量瓶只能用来配制一定体积准确浓度的溶液,不能用于贮存溶液,故B错误;
C.容量瓶不能配制或测量容量瓶规格以下的任意体积的液体,故C错误;
D.容量瓶能准确稀释某一浓度的溶液,故D正确;
E.容量瓶只能用于配制一定浓度的溶液,不能用来加热溶解固体溶质,故E错误;
故答案为:BCE;
(3)需要0.1mol/LNaOH溶液450mL,需要配制500mL 0.1mol/L的氢氧化钠溶液,需要氢氧化钠的物质的量为:0.1mol/L×0.5L=0.05mol,需要氢氧化钠的质量为:40g/mol×0.05mol=2.0g;配制500mL 0.1mol/L的氢氧化钠溶液的步骤为:计算、称量、溶解、冷却、移液、洗涤、定容、摇匀等,所以正确的配制顺序为:BCAFED,
故答案为:2.0;BCAFED;
(4)98%、密度为1.84g/cm3的浓硫酸的物质的量浓度为:
| 1000×1.84×98% |
| 98 |
| 0.5mol/L×0.5L |
| 18.4mol/L |
故答案为:13.6;15.
点评:本题考查了配制一定物质的量浓度的溶液的方法,该题是中等难度的试题,试题基础性强,贴近高考;该题难易适中,注重灵活性,侧重对学生能力的培养和解题方法的指导和训练,有利于培养学生的逻辑思维能力和严谨的规范实验操作能力.

练习册系列答案
 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案
相关题目
下列各微粒的电子式正确的是( )
A、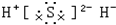 |
B、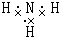 |
C、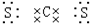 |
D、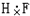 |
 I.写出下列热化学反应方程式
I.写出下列热化学反应方程式