题目内容
10.下列说法正确的是( )| A. | 铅蓄电池工作时,电解质溶液H2SO4的浓度不变 | |
| B. | 加水稀释0.1 mol•L-1CH3COOH溶液时,CH3COOH的电离程度增大,pH减小 | |
| C. | 在同浓度的盐酸中,ZnS可溶而CuS不溶,说明CuS的溶解度比ZnS的小 | |
| D. | 标准状况下,2.24 LCCl4含有的共价键数为0.4×6.02×1023个 |
分析 A.由铅蓄电池的总反应PbO2+2H2SO4+Pb═2PbSO4+2H2O判断;
B.CH3COOH溶液加水稀释,平衡向正反应方向移动,电离程度增大,但溶液体积增大,c(H+)减小;
C.相同条件下,溶解度越小越难溶;
D.标准状况下,CCl4为液态,无法计算.
解答 解:A.由铅蓄电池的总反应PbO2+2H2SO4+Pb═2PbSO4+2H2O可知,硫酸被消耗,电解质H2SO4的浓度减小,故A错误;
B.CH3COOH溶液加水稀释,平衡向正反应方向移动,电离程度增大,但溶液体积增大,则溶液中c(H+)减小,pH增大,故B错误;
C.在同浓度的盐酸中,ZnS可溶而CuS不溶,则说明CuS的溶解度比ZnS的小,故C正确;
D.标准状况下,CCl4为液态,无法计算2.24 LCCl4含有的共价键数,故D错误;
故选C.
点评 本题考查较为综合,涉及电化学、弱电解质的电离、沉淀溶解平衡等知识,题目难度不大,试题培养了学生的灵活应用能力.

练习册系列答案
相关题目
14.能与SO2气体发生反应,但无沉淀产生的是( )
①氯水 ②Ba(OH)2溶液 ③石灰水 ④Na2CO3溶液 ⑤稀硫酸 ⑥Na2SO3溶液.
①氯水 ②Ba(OH)2溶液 ③石灰水 ④Na2CO3溶液 ⑤稀硫酸 ⑥Na2SO3溶液.
| A. | 只有① | B. | ①③④ | C. | ④⑤⑥ | D. | ①④⑥ |
1.以“物质的量”为中心的计算是化学计算的基础,下列与“物质的量”相关的计算正确的是( )
| A. | 现有CO、CO2、O3三种气体,它们分别都含有1 mol O,则三种气体的物质的量之比为3:2:1 | |
| B. | n g Cl2中有m个Cl原子,则阿伏加德罗常数NA的数值可表示为$\frac{35.5m}{n}$ | |
| C. | 标准状况下,11.2 L X气体分子的质量为16 g,则X气体的摩尔质量是32 | |
| D. | 5.6 g CO和22.4 L CO2中含有的碳原子数一定相等 |
18.下列叙述Ⅰ和Ⅱ均正确并且有因果关系的是( )
| 叙述I | 叙述II |
| A.NH4Cl受热易分解 | 可用加热法除去I2中的NH4Cl |
| B.往氯化钙溶液中通入足量的CO2 先有白色沉淀生成,后沉淀溶解 | CaCO3不溶于水,Ca(HCO3)2可溶于水 |
| C.水玻璃具有黏性 | 盛装烧碱溶液的试剂瓶不能用玻璃塞 |
| D.利用丁达尔现象区分氢氧化铁胶体和浓的氯化铁溶液 | 往氢氧化钠溶液中滴加饱和氯化铁溶液,加热至红褐色制得胶体 |
| A. | A | B. | B | C. | C | D. | D |
15.下列有关实验装置(夹持和尾气处理装置已省略)进行的相应实验,不能达到实验目的是( )
| A. | 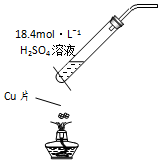 用图装置制取SO2 | |
| B. | 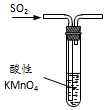 图装置中溶液的颜色变浅,说明SO2具有漂白性 | |
| C. | 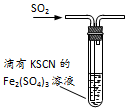 图装置中溶液的颜色变浅,说明SO2具有还原性 | |
| D. |  图装置中产生淡黄色沉淀,说明SO2或H2SO3具有氧化性 |
2.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 30g C2H6中含有的共用电子对数为6NA | |
| B. | 1.0L 1.0mol•L-1Na3PO4水溶液中含有的氧原子数为4NA | |
| C. | 1 mol FeI2与足量氯气反应转移的电子数为3NA | |
| D. | 25℃时,1.0L pH=13的Ba(OH)2溶液中含有的OH-数目为0.2NA |
19.下列说法不正确的是( )
| A. | 用溴水一种试剂可将苯、四氯化碳、乙烯、乙醇、苯酚鉴别开 | |
| B. | 组成为C4H10O的醇与乙二酸在一定条件下生成二元酯的种类有10种 | |
| C. | 二糖、淀粉、纤维素水解的最终产物都是葡萄糖 | |
| D. | 芥子醇结构简式是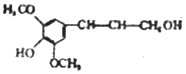 ,则分子中所有碳原子可能在同一平面且与足量溴水反应,最多消耗1molBr2 ,则分子中所有碳原子可能在同一平面且与足量溴水反应,最多消耗1molBr2 |
7.下列关于晶体的说法正确的是( )
| A. | 离子晶体中一定含金属阳离子 | |
| B. | 只要含有金属阳离子的晶体就一定是离子晶体 | |
| C. | 分子晶体的熔点不一定比金属晶体的熔点低 | |
| D. | 在共价化合物分子中,各原子都形成8电子结构 |