题目内容
5.一氧化钴(CoO)是一种重要的工业催化剂,某学习小组欲从含钴废料中(含Co2O3、CoO 和少量Fe、Al)回收一氧化钴,设计工艺流程如下:已知:Co2O3的氧化性>Cl2的氧化性下列说法不正确的是( )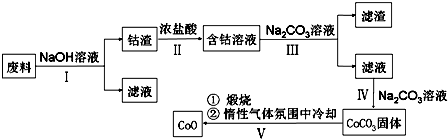
| A. | 第Ⅰ步反应后得到的滤液主要是含铝溶液 | |
| B. | 第Ⅱ步中盐酸表现出酸性、还原性,且必须过量 | |
| C. | 第Ⅲ步中Na2CO3主要作用是使Fe3+沉淀,滤渣主要为Fe(OH)3 | |
| D. | 第Ⅳ步操作为过滤,第Ⅴ步煅烧后,也可以在一氧化碳气体氛围中冷却 |
分析 含钴废料中含有Co2O3、CoO 和少量Fe、Al,向废料中加入NaOH溶液,只有Al和NaOH反应生成可溶性的NaAlO2,然后过滤得到滤渣Co2O3、CoO 和少量Fe,滤液中含有NaOH和NaAlO2,向滤渣中加入浓盐酸,发生反应 Co2O3+6HCl=2CoCl2+Cl2↑+3H2O、Fe+2HCl=FeCl2+H2↑、CoO+2HCl=CoCl2+H2O,得到含有Co的溶液,向溶液中加入碳酸钠溶液得到可溶性的CoCO3和FeCO3沉淀,过滤得到滤渣FeCO3,滤液中含有CoCO3,向滤液中再加入碳酸钠溶液,得到CoCO3固体,将CoCO3在惰性气体中煅烧得到CoO,结合题目分析解答.
解答 解:含钴废料中含有Co2O3、CoO 和少量Fe、Al,向废料中加入NaOH溶液,只有Al和NaOH反应生成可溶性的NaAlO2,然后过滤得到滤渣Co2O3、CoO 和少量Fe,滤液中含有NaOH和NaAlO2,向滤渣中加入浓盐酸,发生反应 Co2O3+6HCl=2CoCl2+Cl2↑+3H2O、Fe+2HCl=FeCl2+H2↑、CoO+2HCl=CoCl2+H2O,得到含有Co的溶液,向溶液中加入碳酸钠溶液得到可溶性的CoCO3和FeCO3沉淀,过滤得到滤渣FeCO3,滤液中含有CoCO3,向滤液中再加入碳酸钠溶液,得到CoCO3固体,将CoCO3在惰性气体中煅烧得到CoO,
A.通过以上分析知,第Ⅰ步反应后得到的滤液主要是含铝溶液,还含有少量NaOH,故A正确;
B.浓盐酸和Co2O3反应体现还原性和酸性,和CoO、Fe反应只体现酸性,故B正确;
C.碳酸根离子和铁离子发生双水解反应生成氢氧化铁红褐色沉淀,故C正确;
D.CO能还原CoO而得不到CoO,故D错误;
故选D.
点评 本题考查物质分离和提纯,为高频考点,侧重考查学生分析判断及思维的缜密性、获取信息解答问题能力,明确流程图中发生的反应及分离提纯方法、物质性质是解本题关键,注意II中发生的反应,题目难度不大.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| 实验编号 | 实验温度/℃ | c(Na2S2O3)/mol•L-1 | c(H2SO4)/mol•L-1 |
| ① | 25 | 0.1 | 0.1 |
| ② | 25 | 0.2 | 0.1 |
| ③ | 25 | 0.1 | 0.2 |
| ④ | 50 | 0.2 | 0.1 |
| ⑤ | 50 | 0.1 | 0.1 |
探究浓度对化学反应速率的影响,应选择①②或①③或④⑤(填实验编号);
若同时选择①②③溶液变浑浊的时间,探究比较改变不同反应物浓度对反应速率的影响对化学反应速率的影响.
| A. | 未知浓度酸液用滴定管量取,滴定管用蒸馏水洗涤后,没用待测酸液润洗 | |
| B. | 装待测液的锥形瓶用蒸馏水洗涤后,没用待测液冲洗 | |
| C. | 量取酸液的体积时,开始仰视凹液面,取液结束时俯视凹液面 | |
| D. | 滴定开始滴定管尖端有气泡,到达终点时尖端无气泡 |
| A. | 有4种不同的伸展方向 | B. | 有5种不同能量的电子 | ||
| C. | 有5种不同的运动范围 | D. | 有14种不同运动状态的电子 |
| A. | 增加FeS2的量 | B. | 增大O2的浓度 | C. | 升高温度 | D. | 减小压强 |
| A. | ⅠA元素的电负性从上到下逐渐减小,ⅦA元素的第一电离能从上到下逐渐减小 | |
| B. | 电负性的大小可以作为衡量元素的金属性和非金属性强弱的尺度 | |
| C. | NaH的存在能支持可将氢元素放在ⅦA的观点 | |
| D. | 氢原子中只有一个电子,故氢原子只有一个原子轨道 |
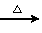 CO2↑+2H2O↑+4Cu。当甲烷完全反应后,硬质玻璃管的质量减轻了4.8g。将反应后气体通入2L0.lmol/L的澄清Ca(OH)2溶液,充分吸收,生成沉淀10g。求:
CO2↑+2H2O↑+4Cu。当甲烷完全反应后,硬质玻璃管的质量减轻了4.8g。将反应后气体通入2L0.lmol/L的澄清Ca(OH)2溶液,充分吸收,生成沉淀10g。求: