题目内容
用铁片与稀H2SO4反应制取H2,下列措施不能使H2的生成速率增大的是( )
| A、加热 |
| B、不用铁片,改用铁粉 |
| C、增加H+的浓度 |
| D、不用稀H2SO4,改用98%的浓H2SO4 |
考点:化学反应速率的影响因素
专题:化学反应速率专题
分析:影响铁与稀硫酸反应的因素有浓度、温度、固体表面积大小以及原电池反应等,一般来说,增大浓度、升高温度、增大固体表面积或形成原电池反应都可增大反应速率.
解答:
解:A.加热,温度升高,活化分子的百分数增大,反应速率增大,故B不选;
B.固体表面积增大,反应速率增大,故B不选;
C.增加H+的浓度会提高反应速率,故C不选;
D.不用稀H2SO4,改用98%的浓H2SO4,铁在浓硫酸中发生钝化阻止反应进行,故D选;
故选D.
B.固体表面积增大,反应速率增大,故B不选;
C.增加H+的浓度会提高反应速率,故C不选;
D.不用稀H2SO4,改用98%的浓H2SO4,铁在浓硫酸中发生钝化阻止反应进行,故D选;
故选D.
点评:本题考查化学反应速率的影响,为高频考点,侧重于学生的分析能力和基本理论知识的综合理解和运用的考查,注意把握影响化学反应速率的影响和影响原因,难度不大,注意相关基础知识的积累.

练习册系列答案
相关题目
下面说法正确的是( )
| A、摩尔是七个基本物理量之一 |
| B、物质的量就是物质的质量 |
| C、摩尔是物质的量的单位 |
| D、阿伏加德罗常数就是6.02×10-23mol-1 |
下列各组离子在指定条件下能大量共存的是( )
| A、无色溶液中:Cu2+、Na+、Cl-、NO3- |
| B、强酸性溶液中:Na+、K+、OH-、Cl- |
| C、含Fe3+的溶液中:K+、Ca2+、NO3-、OH- |
| D、澄清透明溶液中:Fe2+、Na+、SO42-、Cl- |
关于硝酸的说法正确的是( )
| A、硝酸电离出的H+离子,能被Zn、Fe等金属还原成H2 |
| B、常温下,向浓HNO3中投入Fe片,会产生大量的红棕色气体 |
| C、硝酸与金属反应时,主要是+5价的氮得电子 |
| D、浓HNO3与浓HCl按3:1的体积比所得的混合物叫王水 |
168O、188O、O2-、O2、O3是( )
| A、氧元素的五种不同微粒 |
| B、五种氧元素 |
| C、氧的五种同素异形体 |
| D、氧的五种同位素 |
下列关于平衡常数K的说法中,正确的是( )
①平衡常数K只与反应本身及温度有关
②改变反应物浓度或生成物浓度都会改变平衡常数K
③加入催化剂不改变平衡常数K
④平衡常数K只与温度有关,与反应的本身及浓度、压强无关.
①平衡常数K只与反应本身及温度有关
②改变反应物浓度或生成物浓度都会改变平衡常数K
③加入催化剂不改变平衡常数K
④平衡常数K只与温度有关,与反应的本身及浓度、压强无关.
| A、①② | B、②③ | C、③④ | D、①③ |
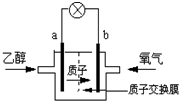 一种新型乙醇电池用磺酸类质子作溶剂,比甲醇电池效率高出32倍.电池总反应为:C2H5OH+3O2=2CO2+3H2O,电池示意图如图.下面对这种电池的说法正确的是( )
一种新型乙醇电池用磺酸类质子作溶剂,比甲醇电池效率高出32倍.电池总反应为:C2H5OH+3O2=2CO2+3H2O,电池示意图如图.下面对这种电池的说法正确的是( )| A、b极为电池的负极 |
| B、设每个电子所带电量为q库仑,则1mol乙醇被氧化产生12NAq库仑的电量 |
| C、电池工作时电流由a极沿导线经灯泡再到b极 |
| D、电池正极的电极反应为:O2+4e-+2H2O=4OH- |
下列说法正确的是( )
| A、分子晶体中一定不含离子键,但一定存在共价键 |
| B、熔融状态下能导电的化合物一定含离子键;金属与非金属元素形成的化合物一定是离子化合物 |
| C、NCl3分子中所有的原子均为8电子稳定结构 |
| D、NaHSO4晶体中阴、阳离子的个数比是1:2,且熔化时破坏的是离子键和共价键 |