题目内容
8.将3.2gCu跟30.0mL、10.0mol•L-1的HN03充分反应,还原产生NO和N02.若反应后溶液中有amolH+离子,则此时溶液中含N03-离子的物质的量为( )| A. | 0.5amol | B. | 0.1amol | C. | (0.1+a)mol | D. | 2amol |
分析 铜与过量的硝酸,反应后溶液中所含H+离子为a mol,说明溶液为Cu(N03)2与HN03的混合溶液,溶液中n(N03-)=n(H+)+2n(Cu2+),据此计算.
解答 解:3.2g铜的物质的量为$\frac{3.2g}{64g/mol}$=0.05mol.
铜与过量的硝酸,反应后溶液中所含H+离子为a mol,说明溶液为Cu(N03)2与HN03的混合溶液,根据电荷守恒溶液中n(N03-)=n(H+)+2n(Cu2+)=amol+0.05mol×2=(a+0.1)mol.
故选:C.
点评 考查氧化还原反应的计算,难度中等,本题不宜采取常规方法计算,判断溶液组成是关键,利用电荷守恒与原子守恒解答.

练习册系列答案
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案
相关题目
19.下列化学实验事实及其解释或结论都正确的是( )
| A. | 蘸有浓氨水的玻璃棒置于某浓无机酸的试剂瓶口,有大量白烟,说明该酸为盐酸 | |
| B. | 向1 mL 1%的NaOH溶液中加入2 mL 2%的CuSO4溶液,振荡后再滴入有机物X,加热至沸后无砖红色沉淀,说明X中不含有醛基 | |
| C. | 向KI淀粉溶液中滴入氯水变蓝,再通入SO2,蓝色褪去,说明SO2具有还原性 | |
| D. | 往盛有漂粉精溶液的试管中滴加浓硫酸,产生黄绿色气体,说明浓硫酸有强氧化性 |
16.与二氧化硫反应时,下列物质作还原剂的是( )
| A. | 氯水 | B. | 硫化氢 | C. | 品红 | D. | 氢氧化钙 |
3.在150℃时,某气态混合烃和过量O2在一密闭容器中完全反应,测知反应前后压强没有变化,则该混合烃可能是( )
| A. | CH4和C2H4 | B. | CH4和C2H6 | C. | C2H4和C2H6 | D. | C3H4和C3H6 |
13.在氯水中存在多种分子和离子,它们在不同的反应中表现出各自的性质.下列实验现象和结论一致且正确的是( )
| A. | 加入有色布条,一会儿有色布条褪色,说明溶液中有Cl2存在 | |
| B. | 溶液呈浅黄绿色,且有刺激性气味,说明有Cl2分子存在 | |
| C. | 氯水滴在PH试纸上,一段时间后将观察到试纸变红,说明H+存在 | |
| D. | 加入NaOH溶液,氯水浅黄绿色消失,说明有HClO分子存在 |
20.已知HCN是直线型结构,下列有机分子中,所有的原子不可能处于同一平面的是( )
| A. | CH2═CH-CN | B. | CH2═CH-CH═CH2 | C. | 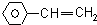 | D. | 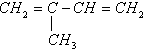 |
17.下列各项中表达正确的是考( )
| A. | CO2的电子式为: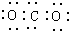 | B. | Cl2的结构式: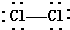 | ||
| C. | 用电子式表示NaCl的形成过程: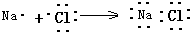 | D. | F-的结构示意图: |
18.在稀溶液在,2ROH(aq)+H2SO4(aq)═R2SO4(aq)+2H2O(l)△H=-24.6 kJ•mol-1,又知稀硫酸与NaOH溶液反应时的中和热为57.3 kJ•mol-1,则ROH(aq)═OH-(aq)+R+(aq)的△H为( )
| A. | +45 kJ•mol-1 | B. | +32.7 kJ•mol-1 | C. | -45 kJ•mol-1 | D. | 无法计算 |
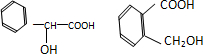 等(写一种即可)
等(写一种即可)