题目内容
4.下列化学用语表述正确的是( )| A. | 原子核内有8个中子的碳原子:${\;}_{8}^{14}$C | |
| B. | NH4Cl的电子式: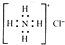 | |
| C. | HClO的结构式:H-Cl-O | |
| D. | Ca2+的结构示意图: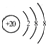 |
分析 A.原子核内有8个中子的碳原子,质子数为6,则质量数=质子数+中子数=14,元素符号的左上角为质量数、左下角为质子数;
B.氯离子为阴离子,应标出最外层电子;
C.HClO分子中氧原子分别与氢原子和氯原子形成公用电子对,形成8电子稳定结构;
D.钙原子核电荷数是20,最外层电子数为2,失去2个电子形成钙离子.
解答 解:A.原子核内有8个中子的碳原子,质子数为6,则质量数=质子数+中子数=14,原子符号为146C,故A错误;
B.氯离子为阴离子,应标出最外层电子,故氯化铵的电子式为 ,故B错误;
,故B错误;
C.次氯酸为共价化合物,分子中存在1个O-H键和1个H-Cl共价键,次氯酸的电子式为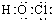 ,结构式为H-O-Cl,故C错误;
,结构式为H-O-Cl,故C错误;
D.钙原子核电荷数是20,最外层电子数为2,失去2个电子形成钙离子,离子结构示意图,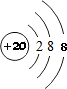 ,故D正确;
,故D正确;
故选D.
点评 本题考查常见化学用语的书写,题目难度不大,本题注意相关基础知识的积累,注意把握在书写电子式之前,先判断化合物是离子化合物还是共价化合物.

练习册系列答案
相关题目
15.某化学反应中,反应物A的模拟过度在5s内由2.0mol/L变成1.5mol/L,在这5s内用A表示化学反应速率为( )
| A. | 0.5mol/L | B. | 0.4mol/(L?s) | C. | 0.3mol/(L?s) | D. | 0.1 mol/(L?s) |
12.下列设备工作时能将电能转化为化学能的是( )
| A. |  硅太阳能电池 | B. |  钠冶炼槽 | C. |  太阳能集热器 | D. |  氢氧燃料电池 |
19.常温常压下,由三种气态烃以任意比例组成混合气体,现取体积为V的该混合气体与足量氧气混合,经点燃爆炸后恢复到原状况,气体总体积缩小了2V.混合烃的可能组合是( )
| A. | CH4C2H4C3H4 | B. | CH4C2H6C2H2 | C. | C2H2C2H4C3H6 | D. | C2H4C3H6C4H8 |
9.已知某有机物X的结构简式如图所示,下列有关叙述不正确的是( )
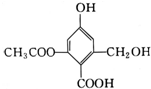

| A. | X的化学式为C10H10O6 | |
| B. | X在一定条件下能与FeCl3溶液发生显色反应 | |
| C. | X在一定条件下能发生消去反应和酯化反应 | |
| D. | 1 mol X分别与足量的Na、NaOH溶液、NaHCO3溶液反应,消耗的物质的量分别为3 mol、4 mol、1 mol |
16.能证明乙醇分子中含有一个羟基的事实是( )
| A. | 乙醇完全燃烧生成水 | |
| B. | 0.1mol CH3CH2OH与足量金属钠反应生成0.05molH2 | |
| C. | 乙醇能与水以任意比例互溶 | |
| D. | 乙醇的沸点(78.5℃)比乙烷(-88.6℃)的高出许多 |
13.原子核外都有3个电子层的A、B、C三种元素,它们形成的离子分别为A+、B2+、C-,则它们的核电荷数从大到小的顺序是( )
| A. | B>A>C | B. | C>B>A | C. | A>B>C | D. | C>A>B |
19.为提纯如表物质(括号内的物质为杂质),所选用的除杂试剂和分离方法都正确的是( )
| A | B | C | D | |
| 被提纯物质 | 酒精(水) | 乙醇(乙酸) | 乙烷(乙烯) | 溴苯(溴) |
| 除杂试剂 | 生石灰 | 氢氧化钠溶液 | 酸性高锰 酸钾溶液 | KI溶液 |
| 分离方法 | 蒸馏 | 分液 | 洗气 | 分液 |
| A. | A | B. | B | C. | C | D. | D |