题目内容
根据下列框图回答问题(答题时,方程式中的M、E用所对应的元素符号表示):
(1)写出M溶于稀硫酸和H2O2混合液的化学方程式: .
(2)写出X→Y的离子方程式: .
(3)①写出Cl2将Z氧化为K2EO4的化学方程式: .
②K2EO4是一种新型的自来水处理剂,它的性质和作用是 .
A.有强氧化性,可消毒杀菌,还原产物能吸附水中杂质
B.有强还原性,可消毒杀菌,氧化产物能吸附水中杂质
C.有强氧化性,能吸附水中杂质,还原产物能消毒杀菌
D.有强还原性,能吸附水中杂质,氧化产物能消毒杀菌.

(1)写出M溶于稀硫酸和H2O2混合液的化学方程式:
(2)写出X→Y的离子方程式:
(3)①写出Cl2将Z氧化为K2EO4的化学方程式:
②K2EO4是一种新型的自来水处理剂,它的性质和作用是
A.有强氧化性,可消毒杀菌,还原产物能吸附水中杂质
B.有强还原性,可消毒杀菌,氧化产物能吸附水中杂质
C.有强氧化性,能吸附水中杂质,还原产物能消毒杀菌
D.有强还原性,能吸附水中杂质,氧化产物能消毒杀菌.
考点:无机物的推断
专题:推断题
分析:红色金属M为Cu,在过氧化氢作用下与硫酸反应可生成CuSO4,Y中加入KSCN溶液呈红色,说明Y为Fe2(SO4)3,则E为Fe,X为FeSO4,由转化关系可知Z为Fe(OH)3,结合物质的性质和题目要求解答该题.
解答:
解:红色金属M与过氧化氢、硫酸反应得到MSO4为蓝色溶液,则应为CuSO4,所以M为Cu.Y加KSCN呈红色,说明Y中含有Fe3+,结合转化关系,可推知E为Fe,X为FeSO4,Y为Fe2(SO4)3,Z为Fe(OH)3,
(1)Cu和稀硫酸不反应,但在H2O2存在条件下,发生氧化还原反应生成硫酸铜和水,反应的化学方程式为Cu+H2O2+H2SO4═CuSO4+2H2O,
故答案为:Cu+H2O2+H2SO4═CuSO4+2H2O;
(2)X→Y的离子方程式为2Fe2++H2O2+2H+═2Fe3++2H2O,故答案为:2Fe2++H2O2+2H+═2Fe3++2H2O;
(3)①根据反应物结合质量守恒可判断出生成物还应有KCl和水,则反应的化学方程式为10KOH+3Cl2+2Fe(OH)3═2K2FeO4+6KCl+8H2O,
故答案为:10KOH+3Cl2+2Fe(OH)3═2K2FeO4+6KCl+8H2O;
②K2FeO4具有强氧化性,可用于杀菌消毒,被还原生成Fe3+,可水解生成具有吸附性的Fe(OH)3,可用于吸附水中杂质,故答案为:A.
(1)Cu和稀硫酸不反应,但在H2O2存在条件下,发生氧化还原反应生成硫酸铜和水,反应的化学方程式为Cu+H2O2+H2SO4═CuSO4+2H2O,
故答案为:Cu+H2O2+H2SO4═CuSO4+2H2O;
(2)X→Y的离子方程式为2Fe2++H2O2+2H+═2Fe3++2H2O,故答案为:2Fe2++H2O2+2H+═2Fe3++2H2O;
(3)①根据反应物结合质量守恒可判断出生成物还应有KCl和水,则反应的化学方程式为10KOH+3Cl2+2Fe(OH)3═2K2FeO4+6KCl+8H2O,
故答案为:10KOH+3Cl2+2Fe(OH)3═2K2FeO4+6KCl+8H2O;
②K2FeO4具有强氧化性,可用于杀菌消毒,被还原生成Fe3+,可水解生成具有吸附性的Fe(OH)3,可用于吸附水中杂质,故答案为:A.
点评:本题考查无机物的推断,题目难度中等,注意根据物质的特殊性质和反应现象作为推断的突破口,注意相关化学方程式的书写.

练习册系列答案
相关题目
下列实验操作或装置错误的是( )
A、 蒸馏 |
B、 过滤 |
C、 萃取 |
D、 转移溶液 |
100mL 6mol/L H2SO4跟过量锌粉反应,在一定温度下,为了减缓反应进行的速度,但又不影响生成氢气的总量,不可向反应物中加入适量的( )
| A、CH3COONa(固体) |
| B、水 |
| C、硫酸钾溶液 |
| D、硝酸钠(固体) |
 化学实验中,如使某步中的有害产物作为另一步的反应物,形成一个循环,就不再向环境排放该种有害物质.例如铬的化合物有以下循环关系:
化学实验中,如使某步中的有害产物作为另一步的反应物,形成一个循环,就不再向环境排放该种有害物质.例如铬的化合物有以下循环关系:下列有关说法中正确的是( )
| A、上述物质中只有Na2CrO4可作氧化剂 |
| B、发生反应⑤,一定要加入氧化剂 |
| C、发生反应①时,消耗Na2Cr2O7与转移的电子的物质的量之比为1:6 |
| D、从反应②来看,CrCl3不能用Cr(OH)3与盐酸反应来制取 |
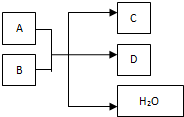 在一定条件下,某些化学反应可用如图表示,请回答下列问题
在一定条件下,某些化学反应可用如图表示,请回答下列问题