题目内容
12.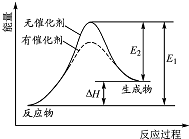 某反应的反应过程中能量变化如图所示(图中E1 表示正反应的活化能,E2 表示逆反应的活化能).下列有关叙述正确的是( )
某反应的反应过程中能量变化如图所示(图中E1 表示正反应的活化能,E2 表示逆反应的活化能).下列有关叙述正确的是( )| A. | 催化剂能改变该反应的焓变 | B. | 催化剂能降低该反应的活化能 | ||
| C. | 该反应为放热反应 | D. | E1 越大,表明该反应越容易发生 |
分析 A、催化剂对反应的焓变无影响;
B、催化剂降低反应的活化能;
C、图象分析反应物能量低于生成物能量,反应是吸热反应;
D、E1为正反应的活化能,E2为逆反应的活化能.
解答 解:A、催化剂对反应的始态和状态无响应,只改变活化能,则对反应的焓变无影响,故A错误;
B、催化剂能改变反应的途径,降低反应的活化能,故B正确;
C、图象分析反应物能量低于生成物能量,反应是吸热反应,故C错误;
D、E1为正反应的活化能,E1 越大,表明该反应越难发生,故D错误.
故选B.
点评 本题考查了化学变化过程中能量变化的分析的,主要是活化能概念的理解应用,掌握图象分析方法是关键,题目较简单.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
2.表是元素周期表的一部分,X、Y、Z、W均为短周期元素,X、Z的质子数之和为21.下列说法正确的是( )
| X | Y | ||
| Z | W |
| A. | X元素不能形成氧化物 | |
| B. | Y元素的最高价氧化物的水化物是含氧酸中酸性最强的 | |
| C. | X元素的非金属性比Y元素非金属性强 | |
| D. | 四种元素中,原子半径最小的元素是Y |
3.下列叙述正确的是( )
| A. | 同一周期元素的原子,半径越小越容易失去电子 | |
| B. | 元素的性质呈周期性变化的根本原因是核外电子排布呈周期性变化 | |
| C. | 第IA族元素与第VIIA族元素形成的化合物都是离子化合物 | |
| D. | 元素周期表中所有元素都是从自然界中发现的,过渡元素都是金属元素 |
20.某元素的离子的结构示意图与Mg2+相同,则下列说法正确的是( )
| A. | 该元素一定在第三周期 | |
| B. | 该元素一定在第二周期 | |
| C. | 若该离子是阳离子,则该元素一定在第三周期 | |
| D. | 若该离子是阴离子,则该元素一定在第三周期 |
17.向密闭容器中充入一定量的N2和H2,发生反应N2(g)+3H2(g)?2NH3(g)△H<0,达到平衡后,要使正反应速率增大,且平衡向正反应方向移动,可采取的措施是( )
| A. | 升温 | B. | 及时分离出氨气 | C. | 加入催化剂 | D. | 增大容器内压强 |
4.下列实验事实解释不合理的是( )
| A. | 乙醇的沸点高于乙醛是因为乙醇分子间存在氢键,而乙醛分子间只有范德华力 | |
| B. | 单质碘易溶于CCl4而微溶于水,是因为I2和CCl4都是非极性分子而水是极性分子 | |
| C. | NH3与CH4的空间构型不同是因为NH3中存在孤电子对而CH4中只有成键电子对 | |
| D. | 水分子比硫化氢稳定是因为水分子存在氢键 |
1.对于合成氨反应N2(g)+3H2(g)?2NH3(g)△H<0;,下列反应速率关系中,正确的是( )
| A. | 3 v (N2)=v(H2) | B. | v (N2)=3v(H2) | C. | 1.5v (H2)=v(NH3) | D. | v (N2)=2v(NH3) |
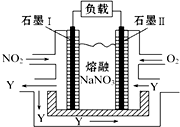 NO2、O2和熔融NaNO3可制作燃料电池,其原理见图,石墨Ⅰ为电池的负极;该电池在使用过程中石墨Ⅰ电极上生成氧化物Y,其电极反应式为NO2-e-+NO3-═N2O5.
NO2、O2和熔融NaNO3可制作燃料电池,其原理见图,石墨Ⅰ为电池的负极;该电池在使用过程中石墨Ⅰ电极上生成氧化物Y,其电极反应式为NO2-e-+NO3-═N2O5.