题目内容
16.2molH2O中含有的氧原子数2mol;氢原子数为4mol.分析 氢原子物质的量为水的2倍,氧原子物质的量等于水的物质的量,根据N=nNA计算水分子数目,由此分析解答;
解答 解:2mol H2O中含H原子为2mol×2=4mol,含有O原子为2mol×1=2mol,故答案为:2;4.
点评 本题考查物质的量有关计算,比较基础,注意对化学式意义的理解,有利于基础知识的巩固.

练习册系列答案
 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案
相关题目
6.A、B、C三种强电解质,它们在水中电离出的离子如表所示:
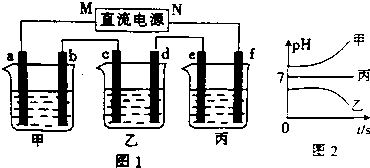
如图1中,甲、乙、丙三个烧杯依次分别盛放足量的A溶液、足量的B溶液、足量的C溶液,电极均为石墨电极.接通电源,经过一段时间后,测得乙中c电极质量增加了16g.常温下各烧杯中溶液的pH与电解时间t的关系如图2.据此回答下列问题:
(1)电极b上发生的电极反应为4OH--4e-=2H2O+O2↑.
(2)写出乙烧杯的电解池总反应化学方程式2CuSO4+2H2O$\frac{\underline{\;通电\;}}{\;}$2Cu+O2↑+2H2SO4.
(3)用惰性电极电解B溶液,当阳离子浓度下降至一半时停止通电,加入下列物质不能使该溶液恢复至起始状态的是C.
A、CuO B、CuO C、Cu(OH)2 D、CuCO3
(4)如果电解过程中B溶液中的金属离子全部析出,此时电解能否继续进行能(填“能”或“不能”).
(5)计算电极e上生成的气体在标准状态下的体积5.6L.
(6)要使丙烧杯溶液恢复到原来的状态,操作是向丙烧杯中加入4.5g水.
| 阳离子 | Na+、K+、Cu2+ |
| 阴离子 | SO${\;}_{4}^{2-}$、OH- |

(1)电极b上发生的电极反应为4OH--4e-=2H2O+O2↑.
(2)写出乙烧杯的电解池总反应化学方程式2CuSO4+2H2O$\frac{\underline{\;通电\;}}{\;}$2Cu+O2↑+2H2SO4.
(3)用惰性电极电解B溶液,当阳离子浓度下降至一半时停止通电,加入下列物质不能使该溶液恢复至起始状态的是C.
A、CuO B、CuO C、Cu(OH)2 D、CuCO3
(4)如果电解过程中B溶液中的金属离子全部析出,此时电解能否继续进行能(填“能”或“不能”).
(5)计算电极e上生成的气体在标准状态下的体积5.6L.
(6)要使丙烧杯溶液恢复到原来的状态,操作是向丙烧杯中加入4.5g水.
7.下列与实验相关的叙述正确的是( )
| A. | 稀释浓硫酸时,应将蒸馏水沿玻璃棒缓慢注入浓硫酸中 | |
| B. | 用浓硫酸配制一定物质的量浓度的硫酸溶液时,溶解后的溶液未冷却至室温就转移入容量瓶,会造成所配溶液浓度偏高 | |
| C. | 溶液加入稀盐酸产生无色气体,将气体通入澄清石灰水,变浑浊,原溶液一定含有CO32- | |
| D. | 检验某溶液是否含有SO42-时,应取少量该溶液,依次加入BaCl2溶液和稀盐酸 |
4.成语是中华民族灿烂文化中的瑰宝,下列涉及氧化还原反应的是( )
| A. | 蜡炬成灰 | B. | 木已成舟 | C. | 铁柱成针 | D. | 滴水成冰 |
11.下列各组物质,前者属于电解质,后者属于非电解质的是( )
| A. | NaCl晶体、BaSO4 | B. | Na2SO4、酒精 | ||
| C. | 铜、二氧化硫 | D. | 熔融的KNO3、硫酸溶液 |
1.氢氧化铝在水中可建立如下平衡:Al3++3OH-?Al(OH)3?H++AlO2-+H2O,运用勒夏特列原理判断,下列叙述中正确的是( )
| A. | 向以上平衡体系中加入足量浓NaOH溶液,两平衡都向右移动,Al(OH)3的质量增加 | |
| B. | 向以上平衡体系中加入足量浓盐酸,Al3+的物质的量增加 | |
| C. | 在同一溶液中,Al3+与OH-能大量共存 | |
| D. | 在同一溶液中,AlO2-与H+能大量共存 |
5.X、Y、Z、W是分别位于第2、3周期的元素,原子序数依次递增.X与Z位于同一主族,Y元素的单质既能与盐酸反应也能与NaOH溶液反应,Z原子的最外层电子数是次外层电子数的一半,Y、Z、W原子的最外层电子数之和为14.下列说法正确的是( )
| A. | 原子半径由小到大的顺序:X<Y<Z<W | |
| B. | X氢化物的沸点高于Z氢化物的沸点 | |
| C. | 最高价氧化物对应水化物的酸性X大于Z | |
| D. | 室温下,0.1 mol/L W的气态氢化物的水溶液的pH>1 |
 .
.