题目内容
锌锰干电池在放电时,电池总反应方程式可表示为:Zn+2MnO2+2NH4+=Zn2++Mn2O3+2NH3+H2O,在电池放电时,正极(碳棒)上发生反应的物质是( )
| A、Zn |
| B、碳棒 |
| C、MnO2和NH4+ |
| D、Zn2+和NH4+ |
考点:原电池和电解池的工作原理
专题:
分析:根据反应式Zn+2MnO2+2NH4+=Zn2++Mn2O3+2NH3+H2O可知,在反应中Zn元素化合价升高,被氧化,Zn为负极反应,Mn元素化合价降低,被还原,MnO2为正极反应,以此解答该题.
解答:
解:在反应中Zn元素化合价升高,被氧化,Zn为负极反应,负极电极反应式为Zn-2e-═Zn2+,Mn元素化合价降低,被还原,MnO2为正极反应,正极反应式为2MnO2+2e-+2NH4+=Mn2O3+2NH3+H2O,由此可知正极上参加反应的物质为MnO2和NH4+,
故选C.
故选C.
点评:本题考查原电池知识,侧重于原电池的电极反应的判断,为高考常见题型,难度不大,注意从化合价的角度分析原电池的两极反应.

练习册系列答案
 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案
相关题目
“84”消毒液在日常生活中使用广泛,该消毒液无色,有漂白作用.它的有效成分是( )
| A、氯化钙溶液 | B、漂白粉溶液 |
| C、次氯酸钠溶液 | D、氯水 |
氢气在氯气中燃烧产生苍白色火焰,在反应中破坏1mol氢气中的化学键消耗的能量为a KJ,破坏1mol 氯气中的化学键消耗的能量为b KJ,形成1mol氯化氢中的化学键释放的能量为c KJ.下列关系式中正确的是( )
| A、a+b>c |
| B、a+b>2c |
| C、a+b<c |
| D、a+b<2c |
汽车的启动电源常用铅蓄电池,放电时的电池反应如下:PbO2+Pb+2H2SO4=2PbSO4↓+2H2O,根据此反应判断下列叙述中正确是( )
| A、PbO2是电池的负极 |
| B、负极的电极反应式为:Pb+SO42--2e -=PbSO4↓ |
| C、PbO2得电子,被氧化 |
| D、电池放电时,溶液酸性增强 |
有关化学用语正确的是( )
| A、氯乙烷的分子式C2H5Cl |
| B、乙醇的结构简式C2H6O |
C、四氯化碳的电子式 |
| D、乙烯的结构简式CH2CH2 |
下列电离方程式中,正确的是( )
| A、Ca(OH)2=Ca2++2(OH-) |
| B、FeCl3=Fe2++3Cl- |
| C、Al2(SO4)3=2Al3++3SO42- |
| D、H2SO4=H2++SO42- |
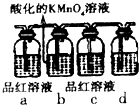 掌握物质之间的转化,是学习元素化合物知识的基础.
掌握物质之间的转化,是学习元素化合物知识的基础.