题目内容
(9分)某同学对MnO2、CuO、Fe2O3、Cr2O3在氯酸钾受热分解反应中的催化作用进行了研究。实验所得数据如下表。就本实验的有关问题,请填空:
| 实验 编号 | KClO3(g) | 氧化物 | 产生气体(mL) (已折算为标况) | 耗时(s) | ||
| 化学式 | 质量(g) | 实际回收 | ||||
| 1 | 0.6 | — | — | — | 10 | 480 |
| 2 | 0.6 | MnO2 | 0.20 | 90% | 67.2 | 36.5 |
| 3 | 0.6 | CuO | 0.20 | 90% | 67.2 | 79.5 |
| 4 | 0.6 | Fe2O3 | 0.20 | 90% | 67.2 | 34.7 |
| 5 | 0.6 | Cr2O3 | 0.20 | 异常 | 67.2 | 188.3 |
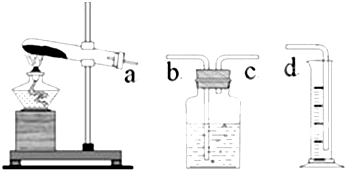
(1)本实验的装置由下图三部分组成,其正确的接口连接顺序为 。
(2)为证明编号2的实验中MnO2起到催化作用,上述实验后还要测定反应剩余物MnO2的质量,实验的操作顺序是:溶解→ → → → 。
(3)从上表实验数据分析,对氯酸钾受热分解有催化作用的物质,按其催化能力从大到小的顺序为 (填物质的化学式)。
(4)从编号3的实验数据,可计算出KClO3的分解率为 %(保留一位小数)。
(5)在进行编号5的实验时,有刺激性的黄绿色气体产生,该气体可能是______(填化学式),常用 试纸检验该气体,上述异常现象产生的原因是 。
(1)a→c→b→d (2)过滤、洗涤、烘干、称量
(3)Fe2O3 >MnO2 > CuO (4)40.8
(5)Cl2;湿润的淀粉碘化钾;氯酸钾在加热条件下将Cr2O3氧化为可溶性化合物
解析:(1)根据装置的特点可判断,通过测量排出水的体积可以计算出生成的氧气体积,所以正确的连接顺序为a→c→b→d。
(2)MnO2不溶于水,所以先溶解,然后过滤、洗涤、烘干,最后称量即可。
(3)收集等量的氧气,耗时最小的,催化效果最好,所以根据有关数值可知,催化能力从大到小的顺序为Fe2O3 > MnO2 > CuO。由于三氧化二铬的质量异常,所以三氧化二铬不是催化剂。
(4)实验3中氧气的物质的量是![]() ,所以消耗氯酸钾的物质的量是0.002mol,质量是0.002mol×122.5g/mol=0.245 g,所以分解率是
,所以消耗氯酸钾的物质的量是0.002mol,质量是0.002mol×122.5g/mol=0.245 g,所以分解率是![]() 。
。
(5)有刺激性的黄绿色气体产生,说明气体是氯气。再根据三氧化二铬的质量异常可判断,在反应过程中氯酸钾被三氧化二铬还原生成了氯气,所以三氧化二铬的质量才会出现异常。

 名校课堂系列答案
名校课堂系列答案(9分)某同学对第四周期过渡元素产生浓厚的兴趣。想探究是否只有MnO2能催化KClO3受热分解?CuO、Fe2O3、Cr2O3等对氯酸钾的受热分解有没有催化作用?若有催化作用,效率怎样?请你与他一起进行实验探究:
I.课题名称:_________________________。
Ⅱ.实验仪器:略
实验试剂:二氧化锰、氧化铁、氧化铜、氧化铬和氯酸钾
Ⅲ.实验步骤:略
Ⅳ.实验数据:
| 实验 编号 | KClO3 (g) | 氧化物 | 产生气体(mL) (已折算为标况) | 耗时(s) | ||
| 化学式 | 质量(g) | 回收 | ||||
| 1 | 0.6 | — | — | — | 10 | 480 |
| 2 | 0.6 | MnO2 | 0.20 | 90% | 67.2 | 36.5 |
| 3 | 0.6 | CuO | 0.20 | 90% | 67.2 | 79.5 |
| 4 | 0.6 | Fe2O3 | 0.20 | 90% | 67.2 | 34.7 |
| 5 | 0.6 | Cr2O3 | 0.20 | 异常 | 67.2 | 188.3 |
⑴请用编号3的实验数据求得KClO3的分解率:为______%(保留一位小数)。
⑵在用Cr2O3做实验时,有刺激性气味的气体产生,同时绿色的混合物变成橘黄色(K2Cr2O7)。该刺激性气体可能是______(填化学式),用 检验。(填序号)
A、湿润的蓝色石蕊试纸 B、湿润的碘化钾淀粉试纸
C、湿润的PH试纸 D、湿润的红色石蕊试纸
Ⅵ.实验结论:________________________________________________________。
(9分)某同学对第四周期过渡元素产生浓厚的兴趣。想探究是否只有MnO2能催化KClO3受热分解?CuO、Fe2O3、Cr2O3等对氯酸钾的受热分解有没有催化作用?若有催化作用,效率怎样?请你与他一起进行实验探究:
I.课题名称:_________________________。
Ⅱ.实验仪器:略
实验试剂:二氧化锰、氧化铁、氧化铜、氧化铬和氯酸钾
Ⅲ.实验步骤:略
Ⅳ.实验数据:
|
实验 编号 |
KClO3 (g) |
氧化物 |
产生气体(mL) (已折算为标况) |
耗时(s) |
||
|
化学式 |
质量(g) |
回收 |
||||
|
1 |
0.6 |
— |
— |
— |
10 |
480 |
|
2 |
0.6 |
MnO2 |
0.20 |
90% |
67.2 |
36.5 |
|
3 |
0.6 |
CuO |
0.20 |
90% |
67.2 |
79.5 |
|
4 |
0.6 |
Fe2O3 |
0.20 |
90% |
67.2 |
34.7 |
|
5 |
0.6 |
Cr2O3 |
0.20 |
异常 |
67.2 |
188.3 |
V.实验讨论:
⑴请用编号3的实验数据求得KClO3的分解率:为______%(保留一位小数)。
⑵在用Cr2O3做实验时,有刺激性气味的气体产生,同时绿色的混合物变成橘黄色(K2Cr2O7)。该刺激性气体可能是______(填化学式),用 检验。(填序号)
A、湿润的蓝色石蕊试纸 B、湿润的碘化钾淀粉试纸
C、湿润的PH试纸 D、湿润的红色石蕊试纸
Ⅵ.实验结论:________________________________________________________。
I.课题名称:______.
Ⅱ.实验仪器:略
实验试剂:二氧化锰、氧化铁、氧化铜、氧化铬和氯酸钾
Ⅲ.实验步骤:略
Ⅳ.实验数据:
| 实验 编号 | KClO3 (g) | 氧化物 | 产生气体(mL) (已折算为标况) | 耗时(s) | ||
| 化学式 | 质量(g) | 回收 | ||||
| 1 | 0.6 | - | - | - | 10 | 480 |
| 2 | 0.6 | MnO2 | 0.20 | 90% | 67.2 | 36.5 |
| 3 | 0.6 | CuO | 0.20 | 90% | 67.2 | 79.5 |
| 4 | 0.6 | Fe2O3 | 0.20 | 90% | 67.2 | 34.7 |
| 5 | 0.6 | Cr2O3 | 0.20 | 异常 | 67.2 | 188.3 |
(1)请用编号3的实验数据求得KClO3的分解率:为______%(保留一位小数).
(2)在用Cr2O3做实验时,有刺激性气味的气体产生,同时绿色的混合物变成橘黄色(K2Cr2O7).该刺激性气体可能是______(填化学式),用______检验.(填序号)
A、湿润的蓝色石蕊试纸 B、湿润的碘化钾淀粉试纸
C、湿润的PH试纸 D、湿润的红色石蕊试纸
Ⅵ.实验结论:______.