题目内容
17.某元素X的近似平均相对原子质量为a,有质量数分别为b和c的两种同位素,则bX和cX在自然界中的原子个数之比为( )| A. | (a-c):(b-a) | B. | (a-c):(b-c) | C. | (a-b):(a-c) | D. | (b-c):(a-c) |
分析 原子的相对原子质量在数值上等于其质量数,元素的相对原子质量是根据元素各种核素的相对原子质量结合各自的丰度计算出的平均值,据此计算.
解答 解:由于一种元素的相对原子质量是用两种同位素的相对原子质量分别乘以各自的丰度计算而得到,设bX和cX的个数比为m:n,则a=b×$\frac{m}{m+n}$+c×$\frac{n}{m+n}$,解得m:n=(a-c):(b-a).
故选A.
点评 本题考查相对原子质量的相关计算,难度不大.要注意元素的相对原子质量是各种同位素的相对原子质量分别乘以各自的丰度.

练习册系列答案
相关题目
8.关于分液漏斗的使用,下列说法正确的是( )
| A. | 可在分液漏斗内用四氯化碳萃取碘酒中的碘单质 | |
| B. | 分液漏斗在使用前只需检查旋塞芯处是否漏水即可 | |
| C. | 放出下层液体时,应打开上方的玻璃塞,并使下端管口紧贴烧杯内壁 | |
| D. | 放出下层液体后,再从漏斗下端口放出上层液体. |
5.要除去下列物质中混有的少量杂质(括号内的物质),所选用的试剂不正确的是( )
| A. | 硫酸钾溶液(碳酸钾)--适量硫酸溶液 | |
| B. | 氯化钠溶液(氯化镁)--适量氢氧化钠溶液 | |
| C. | 氯化钾固体(二氧化硅)--适量氢氧化钾溶液 | |
| D. | 氯气(氯化氢气体)--适量的饱和食盐水 |
12.根据反应(1)~(3),可以判断下列3个物质的氧化性由强到弱的正确顺序是( )
(1)2FeCl3+H2S═2FeCl2+2HCl+S (2)H2S+I2═S+2HI (3)2FeCl3+2HI═2FeCl2+2HCl+I2.
(1)2FeCl3+H2S═2FeCl2+2HCl+S (2)H2S+I2═S+2HI (3)2FeCl3+2HI═2FeCl2+2HCl+I2.
| A. | S>I2>Fe3+ | B. | Fe3+>I2>S | C. | Fe3+>S>I2 | D. | I2>Fe3+>S |
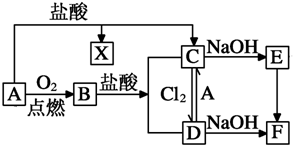
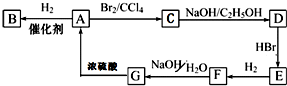 图中A~G均为有机化合物,根据图中的转化关系(反应条件略去),回答下列问题:
图中A~G均为有机化合物,根据图中的转化关系(反应条件略去),回答下列问题:
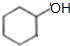 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$ +H2O反应类型是消去反应.由F生成G的化学方程式
+H2O反应类型是消去反应.由F生成G的化学方程式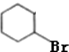 +NaOH$→_{△}^{H_{2}O}$
+NaOH$→_{△}^{H_{2}O}$ +2H2O.
+2H2O.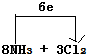 .
.
 .
.