题目内容
向含0.1molNaOH和0.1molBa(OH)2的混合溶液中持续通入CO2气体,则该过程的离子反应方程式为 .
考点:离子方程式的书写
专题:离子反应专题
分析:向含NaOH和Ba(OH)2的混合溶液中持续通入CO2气体,CO2先与Ba(OH)2反应生成BaCO3和H2O,等Ba(OH)2消耗完后,CO2再与NaOH反应生成Na2CO3和水,持续通入CO2,Na2CO3会与CO2反应生成NaHCO3,最后发生BaCO3与CO2反应生成Ba(HCO3)2,然后根据离子方程式的书写方法来书写.
解答:
解:向含NaOH和Ba(OH)2的混合溶液中持续通入CO2气体,CO2先与Ba(OH)2反应生成BaCO3和H2O:CO2+Ba(OH)2=BaCO3↓+H2O,能拆的为Ba(OH)2,故离子方程式为:CO2+Ba2++2OH-=BaCO3↓+H2O;
等Ba(OH)2消耗完后,CO2再与NaOH反应生成Na2CO3和水:CO2+2NaOH=Na2CO3+H2O,其中能拆的物质为:NaOH和Na2CO3,故离子方程式为:CO2+2OH-=CO32-+H2O;
持续通入CO2,Na2CO3会与CO2反应生成NaHCO3:Na2CO3+CO2+H2O=2NaHCO3,能拆的物质为:Na2CO3和NaHCO3,而且NaHCO3只能拆为Na+和HCO3-,故离子方程式为:
CO32-+CO2+H2O=2HCO3-;
最后发生BaCO3与CO2反应生成Ba(HCO3)2:BaCO3+CO2+H2O=Ba(HCO3)2,能拆的物质只有:Ba(HCO3)2,故离子方程式为:BaCO3+CO2+H2O=Ba2++2HCO3-.
故答案为:CO2+Ba2++2OH-=BaCO3↓+H2O;CO2+2OH-=CO32-+H2O;CO32-+CO2+H2O=2HCO3-;BaCO3+CO2+H2O=Ba2++2HCO3-.
等Ba(OH)2消耗完后,CO2再与NaOH反应生成Na2CO3和水:CO2+2NaOH=Na2CO3+H2O,其中能拆的物质为:NaOH和Na2CO3,故离子方程式为:CO2+2OH-=CO32-+H2O;
持续通入CO2,Na2CO3会与CO2反应生成NaHCO3:Na2CO3+CO2+H2O=2NaHCO3,能拆的物质为:Na2CO3和NaHCO3,而且NaHCO3只能拆为Na+和HCO3-,故离子方程式为:
CO32-+CO2+H2O=2HCO3-;
最后发生BaCO3与CO2反应生成Ba(HCO3)2:BaCO3+CO2+H2O=Ba(HCO3)2,能拆的物质只有:Ba(HCO3)2,故离子方程式为:BaCO3+CO2+H2O=Ba2++2HCO3-.
故答案为:CO2+Ba2++2OH-=BaCO3↓+H2O;CO2+2OH-=CO32-+H2O;CO32-+CO2+H2O=2HCO3-;BaCO3+CO2+H2O=Ba2++2HCO3-.
点评:本题考查了离子方程式的书写,应注意反应的先后顺序,难度不大.

练习册系列答案
相关题目
以下各组离子能在给定的四种溶液中大量共存的是( )
| A、加入铁粉产生大量气体的溶液:Cu2+、Na+、Mg2+、NO3- |
| B、滴加酚酞显红色的溶液:Fe3+、NH4+、Cl-、NO3- |
| C、无色透明溶液:K+、SO42-、NO3-、OH- |
| D、碱性溶液:K+、HCO3-、Cl-、Ba2+ |
X2气和Y2气共100mL,一定条件下使它们充分反应,恢复到原状况时,发现体积仍是100mL,这说明( )
| A、X2气过量 |
| B、X2气Y2气各50mL |
| C、产物是双原子分子 |
| D、无法作出上述判断 |
下列叙述中,正确的是( )
| A、1mol气体所占的体积约为22.4L,不一定要在标准状况下 |
| B、在标准情况下,1mol四氯化碳的体积约为22.4L |
| C、直径介于1nm-100nm之间的微粒成为胶体 |
| D、淀粉溶胶中含有少量的NaCl,可用适量的硝酸银溶液除去 |
化学史中许多科学家创建的理论对化学的发展起到重大作用.下列有关科学家及其创建理论的描述中,错误的是( )
| A、拉瓦锡阐明了质量守恒定律 |
| B、道尔顿创立分子学说 |
| C、门捷列夫发现了元素周期律 |
| D、勒沙特列发现化学平衡移动原理 |
下列物质的分离方法不正确的是( )
| A、用过滤的方法除去食盐水中的泥沙 |
| B、用分液法分离酒精和水 |
| C、用四氯化碳萃取碘水中的碘 |
| D、用蒸馏的方法将自来水制成蒸馏水 |
黑火药爆炸反应为:S+2KNO3+3C=K2S+3CO2↑+N2↑,在该反应中,氧化剂是( )
①C ②S ③K2S ④KNO3 ⑤N2.
①C ②S ③K2S ④KNO3 ⑤N2.
| A、①③⑤ | B、②④ |
| C、②④⑤ | D、③④⑤ |
 ,物质A在体内脱氢酶的作用下会氧化为有害物质GHB.下图是关于物质A的一种制备方法及由A引发的一系列化学反应.
,物质A在体内脱氢酶的作用下会氧化为有害物质GHB.下图是关于物质A的一种制备方法及由A引发的一系列化学反应.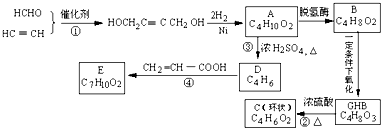
 结构),它的结构简式为
结构),它的结构简式为