题目内容
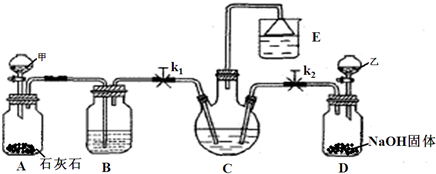
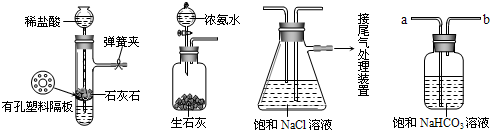
某化学小组模拟“侯氏制碱法”,以NaCl、NH3、CO2和水等为原料以及图1所示装置制取NaHCO3,反应的化学方程式为:
NH3+CO2+H2O+NaCl=NaHCO3+NH4Cl.然后再将NaHCO3制成Na2CO3.
(1)装置乙的作用是
(2)由装置丙中产生的NaHCO3制取Na2CO3时,需要进行的实验操作有
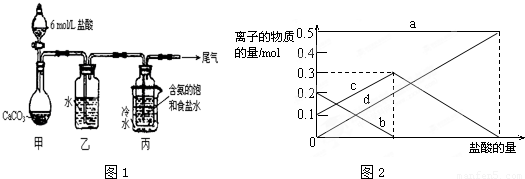
(3)若在(2)中灼烧的时间较短,NaHCO3将分解不完全,该小组对一份加热了t1min的NaHCO3样品的组成进行了研究.取加热了t1min的NaHCO3样品29.6g 完全溶于水制成溶液,然后向此溶液中缓慢地滴加稀盐酸,并不断搅拌.随着盐酸的加入,溶液中有关离子的物质的量的变化如图2所示.则曲线c 对应的溶液中的离子是
(4)若取10.5g NaHCO3固体,加热了t1min后,剩余固体的质量为7.4g.如果把此剩余固体全部加入到200mL 1mol/L的盐酸中,则充分反应后溶液中H+的物质的量浓度为
NH3+CO2+H2O+NaCl=NaHCO3+NH4Cl.然后再将NaHCO3制成Na2CO3.
(1)装置乙的作用是
吸收HCl
吸收HCl
.为防止污染空气,尾气中含有的NH3
NH3
需要进行吸收处理.(2)由装置丙中产生的NaHCO3制取Na2CO3时,需要进行的实验操作有
过滤
过滤
、洗涤、灼烧.(3)若在(2)中灼烧的时间较短,NaHCO3将分解不完全,该小组对一份加热了t1min的NaHCO3样品的组成进行了研究.取加热了t1min的NaHCO3样品29.6g 完全溶于水制成溶液,然后向此溶液中缓慢地滴加稀盐酸,并不断搅拌.随着盐酸的加入,溶液中有关离子的物质的量的变化如图2所示.则曲线c 对应的溶液中的离子是
HCO3-
HCO3-
(填离子符号);该样品中NaHCO3和Na2CO3的物质的量之比是1:2
1:2
.(4)若取10.5g NaHCO3固体,加热了t1min后,剩余固体的质量为7.4g.如果把此剩余固体全部加入到200mL 1mol/L的盐酸中,则充分反应后溶液中H+的物质的量浓度为
0.375mol/L
0.375mol/L
(设溶液体积变化忽略不计).
分析:(1)装置甲是制备二氧化碳,气体中含有氯化氢气体对后续实验产生干扰,需要除去;尾气中含有氨气,不能排到空气中,需要吸收;
(2)装置丙中是氨化的饱和食盐水中通入二氧化碳生成碳酸氢钠晶体,通过过滤得到晶体洗涤灼烧得到碳酸钠;
(3)混合物是碳酸钠和碳酸氢钠,滴入盐酸发生反应CO32-+H+=HCO3-; HCO3-+H+=CO2↑+H2O;依据图象分析碳酸根离子减小,碳酸氢根离子增多;
(4)依据反应前后质量变化是碳酸氢钠分解的原因,依据反应前后质量变化计算反应的碳酸氢钠和生成的碳酸钠,结合试样质量计算剩余碳酸氢钠,计算得到混合物反应消耗的氢离子得到;
(2)装置丙中是氨化的饱和食盐水中通入二氧化碳生成碳酸氢钠晶体,通过过滤得到晶体洗涤灼烧得到碳酸钠;
(3)混合物是碳酸钠和碳酸氢钠,滴入盐酸发生反应CO32-+H+=HCO3-; HCO3-+H+=CO2↑+H2O;依据图象分析碳酸根离子减小,碳酸氢根离子增多;
(4)依据反应前后质量变化是碳酸氢钠分解的原因,依据反应前后质量变化计算反应的碳酸氢钠和生成的碳酸钠,结合试样质量计算剩余碳酸氢钠,计算得到混合物反应消耗的氢离子得到;
解答:解:(1)装置甲是制备二氧化碳气体的反应装置,生成的二氧化碳气体中含有氯化氢气体,对制备碳酸氢钠有影响,装置乙的作用是吸收氯化氢气体;最后的尾气中含有氨气不能排放到空气中,需要进行尾气吸收;
故答案为:吸收HCl;NH3;
(2)由装置丙中产生的NaHCO3发生的反应为,NH3+CO2+H2O+NaCl=NaHCO3↓+NH4Cl;制取Na2CO3时需要过滤得到晶体,洗涤后加热灼烧得到碳酸钠;
故答案为:过滤;
(3)若在(2)中灼烧的时间较短,NaHCO3将分解不完全,该小组对一份加热了t1min的NaHCO3样品的组成进行了研究.取加热了t1min的NaHCO3样品29.6g 完全溶于水制成溶液,然后向此溶液中缓慢地滴加稀盐酸,并不断搅拌.随着盐酸的加入,发生反应 CO32-+H+=HCO3-; HCO3-+H+=CO2↑+H2O;溶液中有关离子的物质的量的变化为碳酸根离子减小,碳酸氢根离子浓度增大,当碳酸根离子全部转化为碳酸氢根离子,再滴入盐酸和碳酸氢根离子反应生成二氧化碳,碳酸氢根离子减小,所以c曲线表示的是碳酸氢根离子浓度变化;碳酸根离子浓度0.2mol/L;碳酸氢根离子浓度为0.1mol/L;样品中NaHCO3和Na2CO3的物质的量之比是1:2;
故答案为:HCO3-; 1:2;
(4)若取10.5g NaHCO3固体物质的量=
=0.125mol,加热了t1min后,剩余固体的质量为7.4g.依据化学方程式存在的质量变化计算:
2NaHCO3=Na2CO3+CO2↑+H2O△m
2 1 62
0.1mol 0.05mol 10.5g-7.4g
反应后NaHCO3物质的量=0.125mol-0.1mol=0.025mol;NaHCO3+HCl=NaCl+H2O+CO2↑;消耗氯化氢物质的量0.025mol;
Na2CO3物质的量=0.05mol,Na2CO3+2HCl=2NaCl+H2O+CO2↑,消耗氯化氢物质的量0.1mol;
剩余氯化氢物质的量=0.200L×1mol/L-0.025mol-0.1mol=0.075mol,剩余溶液中c(H+)=
=0.375mol/L
故答案为:0.375mol/L
故答案为:吸收HCl;NH3;
(2)由装置丙中产生的NaHCO3发生的反应为,NH3+CO2+H2O+NaCl=NaHCO3↓+NH4Cl;制取Na2CO3时需要过滤得到晶体,洗涤后加热灼烧得到碳酸钠;
故答案为:过滤;
(3)若在(2)中灼烧的时间较短,NaHCO3将分解不完全,该小组对一份加热了t1min的NaHCO3样品的组成进行了研究.取加热了t1min的NaHCO3样品29.6g 完全溶于水制成溶液,然后向此溶液中缓慢地滴加稀盐酸,并不断搅拌.随着盐酸的加入,发生反应 CO32-+H+=HCO3-; HCO3-+H+=CO2↑+H2O;溶液中有关离子的物质的量的变化为碳酸根离子减小,碳酸氢根离子浓度增大,当碳酸根离子全部转化为碳酸氢根离子,再滴入盐酸和碳酸氢根离子反应生成二氧化碳,碳酸氢根离子减小,所以c曲线表示的是碳酸氢根离子浓度变化;碳酸根离子浓度0.2mol/L;碳酸氢根离子浓度为0.1mol/L;样品中NaHCO3和Na2CO3的物质的量之比是1:2;
故答案为:HCO3-; 1:2;
(4)若取10.5g NaHCO3固体物质的量=
| 10.5g |
| 84g/mol |
2NaHCO3=Na2CO3+CO2↑+H2O△m
2 1 62
0.1mol 0.05mol 10.5g-7.4g
反应后NaHCO3物质的量=0.125mol-0.1mol=0.025mol;NaHCO3+HCl=NaCl+H2O+CO2↑;消耗氯化氢物质的量0.025mol;
Na2CO3物质的量=0.05mol,Na2CO3+2HCl=2NaCl+H2O+CO2↑,消耗氯化氢物质的量0.1mol;
剩余氯化氢物质的量=0.200L×1mol/L-0.025mol-0.1mol=0.075mol,剩余溶液中c(H+)=
| 0.075mol |
| 0.2L |
故答案为:0.375mol/L
点评:本题考查了 工业制纯碱的原理分析,生产过程中的物质变化,混合物成分的分析判断和计算应用,实验过程分析,除杂操作,尾气吸收,图象定量分析判断,题目难度中等.

练习册系列答案
相关题目