题目内容
11.制备单质硅时,在高温下发生的主要化学反应如下:①SiO2+2C═Si+2CO↑
②Si+2Cl2═SiCl4
③SiCl4+2H2═Si+4HCl
下列对上述三个反应的叙述正确的是( )
| A. | ①②③均为置换反应 | |
| B. | ①②③均为氧化还原反应 | |
| C. | 在工业生产中若只发生反应①,则在产品硅中可能混有SiC | |
| D. | 三个反应的反应物中硅元素均被氧化 |
分析 A、置换反应是一种单质和一种化合物反应生成另一种单质和化合物的反应,依据概念和反应分析判断;
B、氧化还原反应是反应前后有元素化合价变化的反应;
C、在工业生产中若只发生反应①,SiO2+2C═Si+2CO↑,碳可能还有二氧化硅生成碳化硅;
D、氧化还原反应中元素化合价升高失去电子被氧化.
解答 解:A、①SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑;②Si+2Cl2═SiCl4化合反应,③SiCl4+2H2$\frac{\underline{\;高温\;}}{\;}$Si+4HCl,故A错误;
B、①SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑,反应前后有元素化合价变化; ②Si+2Cl2$\frac{\underline{\;高温\;}}{\;}$SiCl4 反应前后有化合价变化; ③SiCl4+2H2$\frac{\underline{\;高温\;}}{\;}$Si+4HCl,反应前后有元素化合价变化,故B正确;
C、在工业生产中若只发生反应①,SiO2+2C═Si+2CO↑,碳可能还有二氧化硅生成碳化硅,SiO2+3C$\frac{\underline{\;高温\;}}{\;}$SiC+2CO↑,则在产品硅中可能混有SiC,故C正确;
D、①SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑反应前后硅元素化合价降低被还原; ②Si+2Cl2$\frac{\underline{\;高温\;}}{\;}$SiCl4 反应前后硅元素化合价升高,被氧化; ③SiCl4+2H2$\frac{\underline{\;高温\;}}{\;}$Si+4HCl,反应前后硅元素化合价降低,被还原,故D错误;
故选BC.
点评 本题考查了氧化还原反应的概念分析及特征应用,硅及其化合物性质的应用,分析反应中元素化合价的变化是解题关键,题目难度不大.

| A. | 一定有乙烷 | B. | 一定有甲烷 | C. | 一定没有甲烷 | D. | 不一定有甲烷 |
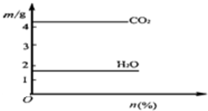 将气体甲通入液体乙中得一混合液,取一定质量的该混合液进行完全燃烧实验,生成CO2、H2O的质量与甲气体在混合液中质量分数关系如图所示,甲、乙组合正确的是( )
将气体甲通入液体乙中得一混合液,取一定质量的该混合液进行完全燃烧实验,生成CO2、H2O的质量与甲气体在混合液中质量分数关系如图所示,甲、乙组合正确的是( )| A. | 乙烯、环己烷 | B. | 甲烷苯 | C. | 乙炔苯 | D. | 乙烷乙醇 |
| A. | 右上方区域的非金属元素 | |
| B. | 过渡区域的金属元素 | |
| C. | 金属元素和非金属元素分界线附近的元素 | |
| D. | 稀有气体元素 |
| A. | H2O2→O2 | B. | SO2→SO32- | C. | Cl2→HCl | D. | HNO3→NO2 |
| A. | C5H12 | B. | (C6H10O5)n | C. | C6H12O6 | D. | C12H22O11 |
| A. | 超导金属 | B. | 形状记忆金属 | C. | 储氢金属 | D. | 光纤 |
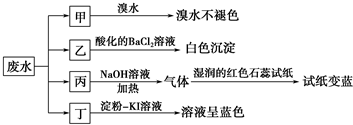
已知废水试样中可能含有下表中的离子:
| 阳离子 | Na+、Mg2+、X |
| 阴离子 | Cl-、SO32-、Y、NO3- |
(2)表中不能确定是否存在的阴离子是Cl-,能证明该阴离子是否存在的简单实验操作为取少量废水试样,滴加足量的Ba(NO3)2溶液,静置,取上层清液,滴加硝酸酸化的AgNO3溶液,若有白色沉淀产生,则存在Cl-,若无白色沉淀产生,则不存在.
(3)丁组实验在酸性条件下发生反应的离子方程式是6I-+2NO3-+8H+=2NO↑+3I2+4H2O.
| A. | 在浓硫酸作催化剂时,可与硝酸发生反应 | |
| B. | 分子中含有三个C-C键和三个C=C键 | |
| C. | 分子中C、H元素的质量比为6:1 | |
| D. | 能使酸性高锰酸钾溶液褪色 |